题目内容
【题目】取一定质量的均匀固体混合物Cu、Cu2O和CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20g,另一份加入1000mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体2.24L,则所用硝酸的物质的量浓度为( )
A.0.8mol/L
B.1.6mol/L
C.0.9mol/L
D.1.8mol/L
【答案】A
【解析】解:取一定质量的均匀固体混合物Cu、Cu2O和CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20g,减少的即为混合物中的O原子的质量,即n(O)= ![]() =0.2mol,而由于在混合物中氧元素的价态为﹣2价,可知混合物中铜元素所带正电荷为0.4mol.而混合物和硝酸反应后生成NO体积为2.24L即0.1mol,可知混合物共失去0.3mol电子,并生成Cu(NO3)2 , 即所得Cu(NO3)2中铜元素所带正电荷的物质的量之和为0.7mol,故做酸的硝酸的物质的量为0.7mol,而由于硝酸在反应时的作用有两个:做酸和做氧化剂,故可知,硝酸的总物质的量为0.7mol+0.1mol=0.8mol.
=0.2mol,而由于在混合物中氧元素的价态为﹣2价,可知混合物中铜元素所带正电荷为0.4mol.而混合物和硝酸反应后生成NO体积为2.24L即0.1mol,可知混合物共失去0.3mol电子,并生成Cu(NO3)2 , 即所得Cu(NO3)2中铜元素所带正电荷的物质的量之和为0.7mol,故做酸的硝酸的物质的量为0.7mol,而由于硝酸在反应时的作用有两个:做酸和做氧化剂,故可知,硝酸的总物质的量为0.7mol+0.1mol=0.8mol.
而硝酸的体积为1L,故硝酸的物质的量浓度为c= ![]() =0.8mol/L,
=0.8mol/L,
故选A.
取一定质量的均匀固体混合物Cu、Cu2O和CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20g,减少的即为混合物中的O原子的质量,据此求出n(O),根据在混合物中氧元素的价态为﹣2价,可知混合物中铜元素的价态之和;然后根据和硝酸反应后生成NO0.1mol,可知混合物共失去0.3mol电子,并生成Cu(NO3)2 , 从而求出混合物反应后的价态,即可求出做酸的硝酸的物质的量,从而求出硝酸的总物质的量和物质的量浓度.

【题目】短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是
X | ||
Y | ||
Z |
A. X,Y,Z中X的单质最稳定B. Y的氢化物为HY
C. X能生成HXOD. 能发生Cl2+H2Z = Z+2HCl的反应
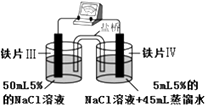
【题目】某同学做如表实验:下列说法正确的是( )
装 |
|
|
现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
A.“电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀
B.铁片Ⅳ的电极反应式可能为Fe﹣3e﹣=Fe3+
C.用K3Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断装置的正、负极
D.铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,所以二者的腐蚀速率相等
【题目】无水AlCl3是一种重要的化工原料.某课外探究小组尝试制取无水AlCl3 , 查阅资料获得下列信息:无水AlCl3在178℃升华,极易潮解,遇水蒸气产生白色烟雾.
探究一 无水AlCl3的实验室制备
利用如图装置,用干燥、纯净的氯气在加热条件下与铝粉(已除去氧化膜)反应制取无水AlCl3 . 供选择的药品:①铝粉 ②浓硫酸 ③稀盐酸 ④饱和食盐水 ⑤二氧化锰粉末 ⑥无水氯化钙 ⑦稀硫酸 ⑧浓盐酸 ⑨氢氧化钠溶液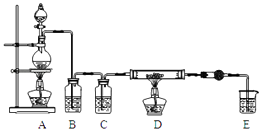
(1)写出装置A烧瓶中发生的反应方程式 .
(2)实验开始前,先检查装置气密性,后装入药品,接下来的步骤依次是(填序号)
a.加热D中硬质玻璃管 b.往A烧瓶中加入液体 c.点燃A中的酒精灯
(3)写出无水AlCl3与水蒸气反应的化学方程式 .
探究二 无水AlCl3的含量测定及结果分析
取D中反应后所得固体2.0g,与足量氢氧化钠溶液反应,测定生成气体的体积(体积均换算成标准状况),重复测定三次,数据如表:
第一次实验 | 第二次实验 | 第三次实验 | |
D中固体用量 | 2.0g | 2.0g | 2.0g |
氢气的体积 | 334.5mL | 336.0mL | 337.5mL |
(4)根据表中数据,计算所得固体中无水AlCl3的质量分数 .
(5)有同学认为测得的无水AlCl3的质量分数偏低,你认为可能的原因有:(填序号)
①制备的氯气不足,②固体和气体无法充分接触,③无水AlCl3发生升华,造成损失.