题目内容
【题目】某同学用胆矾晶体(CuSO4·5H2O)配制0.040mol/L的CuSO4溶液240mL,回答下列问题:
(1)所需仪器为:托盘天平、药匙、烧杯、量筒、胶头滴管,还需要哪些玻璃仪器才能完成该实验?请写出:__________。
(2)请写出该实验的简要的实验步骤:
①计算②称量胆矾_________g③_________④转移⑤洗涤并转移⑥定容⑦摇匀
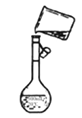
(3)下图是该同学转移溶液的示意图,图中的错误是________。
(4)该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响_________(填“偏高”、“偏低”或“无影响”)。
(5)另有一瓶配制好的CuCl2溶液,因时间过长,标签污损,为检验它就是盛有CuCl2溶液,请写出实验操作及现象。
鉴别对象 | 实验操作、现象 |
Cu2+ | |
Cl- |
【答案】(1)250mL容量瓶、玻璃棒(每项正确得1分,共2分)
(2)②2.5(1分)③溶解(或溶解并恢复至室温)(1分)
(3)转移溶液时不能直接倾倒,应用玻璃棒引流(1分)
(4)偏低(1分)
(5)
鉴别对象 | 实验操作、现象 |
Cu2+ | 取少量待测溶液于试管中,滴入几滴NaOH溶液(1分), 有蓝色沉淀生成(1分)。 |
Cl- | 取少量待测溶液于试管中,加入稀硝酸酸化(1分), 再滴入几滴硝酸银溶液,有白色沉淀生成(1分)。 |
【解析】试题分析:(1)所需仪器有一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀。所以所需仪器有托盘天平、烧杯、玻璃棒、250mL容量瓶、胶头滴管,根据提供的仪器可知,还需要的仪器有250mL容量瓶、玻璃棒。
(2)该实验的简要的实验步骤:①计算;②称量胆矾m=0.25L×0.04molL-1×250g/mol=2.5g;③溶解;④转移; ⑤洗涤并转移;⑥定容 ⑦摇匀。
(3)图中的错误为转移溶液时不能直接倾倒,应用玻璃棒引流。
(4)定容后再加蒸馏水,会使溶液体积偏大,所配溶液浓度偏低。
(5)根据Cl-、Cu2+的检验方法设计实验如下:
鉴别对象 | 实验操作、现象 |
Cu2+ | 取少量待测溶液于试管中,滴入几滴NaOH溶液, 有蓝色沉淀生成。 |
Cl- | 取少量待测溶液于试管中,加入稀硝酸酸化, 再滴入几滴硝酸银溶液,有白色沉淀生成。 |