题目内容
某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置(部分夹持装置已略去):
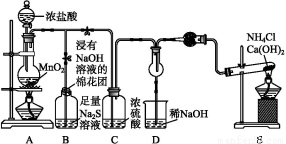
(1)写出A中反应的离子方程式 。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式 。
(3)D中干燥管中出现的现象是 ,化学方程式 。
(4)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,请指出洗气装置盛装试剂 。
(5)还有什么方法能证明氧化性Cl2>S ,用一种相关事实说明 。
(1)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)S2-+Cl2 S↓+2Cl-
S↓+2Cl-
(3)产生大量白烟,8NH3+3Cl2 6NH4Cl+N2
6NH4Cl+N2
(4)饱和食盐水 (6)略
【解析】
试题分析:(1)A为实验室制取氯气的反应,离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)B中出现黄色浑浊现象,说明氯气与硫化钠反应有硫单质生成,离子方程式为2-+Cl2 S↓+2Cl-
S↓+2Cl-
(3)E中产生氨气,经干燥的氯气与氨气反应有不是固体氯化铵生成,所以D中有白烟产生,化学方程式为8NH3+3Cl2 6NH4Cl+N2
6NH4Cl+N2
(4)因为浓盐酸易挥发,若不除去,与氨气发生化合反应生成氯化铵,也有白烟出现,不能证明氯气与氨气发生了氧化还原反应,所以在C前加一洗气装置,洗气装置盛装试剂为饱和食盐水
(5)证明氧化性Cl2>S,可以比较高氯酸与硫酸的酸性强弱。
考点:考查氯、硫非金属性的比较,氯气的实验室制法,离子方程式、化学方程式的书写,实验现象的判断分析

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目