题目内容
将KClO3、I2各0.02 mol加入12 g 36.5%的盐酸中,I2恰好完全溶解,没有气体产生(不考虑盐酸的挥发)。将反应后的溶液用冰水冷却,析出橙红色晶体A(A在常温下就有升华现象),将过滤后的溶液蒸干,收集到KCl固体、8.7g液态水和极少量的A蒸气。则A的化学式可能是
| A.IClO | B.ICl3 | C.I2Cl6 | D.KIO3 |
BC
试题分析:根据题中信息,KClO3、I2等物质的量发生了氧化还原反应,根据电子守恒,KClO3作氧化剂,还原产物中有氯离子生成,碘作还原剂,碘元素化合价升高。假设有1molKClO3反应,转移6mol电子,必将有1mol碘参加反应,产物中碘的化合价是+3价, B.ICl3和 C.I2Cl6 都满足,选BC。

练习册系列答案
相关题目

 C对应的化学方程式 。
C对应的化学方程式 。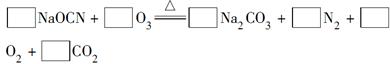
 提供能量。下列有关叙述正确的是( )
提供能量。下列有关叙述正确的是( )
 Cr2O72—(橙色)+H2O下列说法错误的是
Cr2O72—(橙色)+H2O下列说法错误的是 2 K2S + K2SO3 + 3 H2O
2 K2S + K2SO3 + 3 H2O mol的S
mol的S