题目内容
【题目】在 2L 密闭容器中,3mol A 和 1molB 发生反应:3A(g)+B(g)2C(g)+2D(g),10s 末时,生成 1.2mol C,下列说法正确的是
A.10s 内,v(D)=0.12 mol/(L·s)B.10s 末时,物质 A 的转化率为 60%
C.10s 末时,B的浓度为0.3mol/LD.10s 末时,C 的物质的量分数为 15%
【答案】B
【解析】
A.由反应可知,生成1.2molC的同时也生成1.2molD,则v(D)=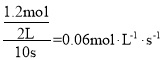 ,故A错误;
,故A错误;
B.由变化量之比等于化学计量数之比可得,生成1.2molC时,消耗的A的物质的量为1.8mol,则A的转化率=![]() ,故B正确;
,故B正确;
C.由变化量之比等于化学计量数之比可得,生成1.2molC时,消耗的B的物质的量为0.6mol,则剩余的B的物质的量为1mol-0.6mol=0.4mol,B的浓度为0.2mol/L,故C错误;
D.由以上分析可知,平衡时A的物质的量为3mol -1.8mol=1.2mol,B的物质的量为0.4mol,C和D的物质的量均为1.2mol,则C 的物质的量分数为=![]() ,故D错误;
,故D错误;
故选:B。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1L的密闭容器中,发生如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是( )
A. T2时,NO2的平衡转化率为70.0%
B. 该反应的△H>0、T1<T2
C. 保持其他条件不变,T1时向平衡体系中再充入0.30molCH4和0.80molH2O(g),平衡向正反应方向移动
D. 保持其他条件不变,T1时向平衡体系中再充入0.50molCH4和1.20molNO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小
【题目】下列实验不能达到实验目的的是( )
序号 | 实验操作 | 实验目的 |
A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
B | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
C | 测定等物质的量浓度的H2CO3、H2SO4溶液的pH | 比较碳、硫的非金属性强弱 |
D | Fe、Cu分别放入相同浓度的盐酸中 | 比较铁、铜的金属性强弱 |
A.AB.BC.CD.D