题目内容
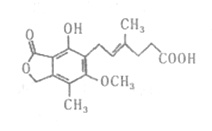
【题目】某可逆反应为:A(g)+B(g)2C(g)+2D(s)△H>0,已知该反应在K=1×10﹣2请回答:
(1)该反应的平衡常数表达式为 .
(2)T℃,若密闭容器中A、B、C的浓度分别为2.5×10﹣1molL﹣1、4.0×10﹣2molL﹣1和3.0×10﹣2molL﹣1 , 此时反应(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是 .
(3)T℃时,向1L密闭容器中充入A和B各1mol,平衡时B的转化率是%(保留一位小数),此时体系内的压强与反应前的压强比为 .
(4)向恒温恒容的密闭容器中充入1molA和1molB,达到平衡状态后再向其中充入2molC和3molD,重新达到化学平衡状态.与原平衡状态相比,此时平衡混合气体中C的体积分数(填“变大”、“变小”、“不变”或“无法判断”).
(5)将A、B的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是(填字母序号).
【答案】
(1)![]()
(2)向逆反应方向进行;![]() =0.09>K=1×10﹣2
=0.09>K=1×10﹣2
(3)4.8;1:1
(4)不变
(5)①④
【解析】解:(1)A(g)+B(g)2C(g)+2D(s)的化学平衡常数表达式K= ![]() , 所以答案是:
, 所以答案是: ![]() ;(2)浓度商Qc=
;(2)浓度商Qc= ![]() =0.09>K=1×10﹣2 , 反应向逆反应方向进行,
=0.09>K=1×10﹣2 , 反应向逆反应方向进行,
所以答案是:向逆反应方向进行; ![]() =0.09>K=1×10﹣2;(3)T℃时,向1L密闭容器中充入A和B各1mol,设平衡时转化的B为xmol,则:
=0.09>K=1×10﹣2;(3)T℃时,向1L密闭容器中充入A和B各1mol,设平衡时转化的B为xmol,则:
A(g)+B(g)2C(g)+2D(s)
开始(mol):1 1 0
转化(mol):x x 2x
平衡(mol):1﹣x 1﹣x 2x
则 ![]() =1×10﹣2 , 解得x=
=1×10﹣2 , 解得x= ![]() ,故B的转化率为
,故B的转化率为 ![]() ×100%=4.8%,恒温恒压下,压强之比等于物质的量之比,反应前后气体的物质的量不变,则此时体系内的压强与反应前的压强比为1:1,所以答案是:4.8;1:1;(4)向恒温恒容的密闭容器中充入1molA和1molB,达到平衡状态后再向其中充入2molC和3molD,等效为开始加入2molA、2molB、1molD,D为固体,不影响平衡移动,由于反应前后气体的物质的量不变,A、B的物质的量之比为1:1,则与原平衡为等效平衡,与原平衡状态相比,此时平衡混合气体中C的体积分数不变,所以答案是:不变;(5)①正反应为吸热反应,升高温度,平衡正向移动,平衡常数增大,图象符合,故正确;②催化剂加快反应速率,缩短到达平衡的水解,但不影响平衡移动,图象中影响平衡移动,故错误;③压强P2先到达平衡,则压强P2>P1 , 反应气体气体的体积不变,压强不影响平衡移动,而图象中压强影响平衡移动,故错误;④混合气体物质的量不变,随反应进行混合气体总质量减小,平均相对分子质量减小,到达平衡后不变,图象符合,故正确,
×100%=4.8%,恒温恒压下,压强之比等于物质的量之比,反应前后气体的物质的量不变,则此时体系内的压强与反应前的压强比为1:1,所以答案是:4.8;1:1;(4)向恒温恒容的密闭容器中充入1molA和1molB,达到平衡状态后再向其中充入2molC和3molD,等效为开始加入2molA、2molB、1molD,D为固体,不影响平衡移动,由于反应前后气体的物质的量不变,A、B的物质的量之比为1:1,则与原平衡为等效平衡,与原平衡状态相比,此时平衡混合气体中C的体积分数不变,所以答案是:不变;(5)①正反应为吸热反应,升高温度,平衡正向移动,平衡常数增大,图象符合,故正确;②催化剂加快反应速率,缩短到达平衡的水解,但不影响平衡移动,图象中影响平衡移动,故错误;③压强P2先到达平衡,则压强P2>P1 , 反应气体气体的体积不变,压强不影响平衡移动,而图象中压强影响平衡移动,故错误;④混合气体物质的量不变,随反应进行混合气体总质量减小,平均相对分子质量减小,到达平衡后不变,图象符合,故正确,
故选:①④.
【考点精析】利用化学平衡状态本质及特征和化学平衡的计算对题目进行判断即可得到答案,需要熟知化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案【题目】某硫酸工业废渣的主要成分为SiO2、MgO、Al2O3、Fe2O3等。回收废渣中金属元素的工艺流程如下:
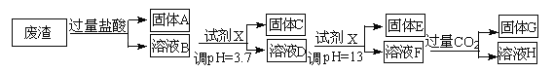
已知常温条件下:
①阳离子以氢氧化物形式开始沉淀和恰好完全沉淀(阳离子浓度等于10-5mol·L-1 )时的pH 如下表所
示。
阳离子 | Fe3+ | Al3+ | Mg2+ |
开始沉淀时的pH | 1.9 | 3.7 | 9.6 |
恰好完全沉淀时的pH | 3.2 | 5.2 | 11.0 |
②饱和氨水溶液中c(OH-)约为1×10-3mol·L-1。
请回答下列问题:
(1)固体C为_________(填化学式)。
(2)上述流程中两次使用试剂X,试剂X是_________(填“氨水”或“氢氧化钠”),其理由是_________________。
(3)溶液D→固体E的过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是________________。
(4)写出溶液F→溶液H 的离子方程式:__________________。
(5)Ksp[Mg (OH )2]=_____________。