题目内容
(14分)I向一金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,解释上述变化的实验现象:
(1)罐壁内凹而瘪的原因:
反应方程式:
(2)罐壁重新鼓起的原因:
反应方程式:
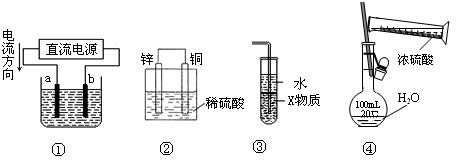
II某学生课外活动小组利用如图所示装置分别做如下实验:

(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是 。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________溶液;加热时溶液由无色变为红色的原因是________________________________。
(1)罐壁内凹而瘪的原因:
反应方程式:
(2)罐壁重新鼓起的原因:
反应方程式:
II某学生课外活动小组利用如图所示装置分别做如下实验:

(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是 。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________溶液;加热时溶液由无色变为红色的原因是________________________________。
I .(1)CO2溶于NaOH溶液而导致罐内压强减小,罐壁被大气压压痹; CO2+2NaOH= Na2CO3+H1O;(2)过量的 NaOH和罐壁(Al)反应而产生H2使罐内压强增大而将罐壁重新鼓起;2Al+2NaOH+2H2O=2NaAlO2+3H2(各2分)
II(1)稀氨水和酚酞(1分);稀氨水中的NH3逸出,碱性减弱,所以溶液的颜色变浅(2分);(2)溶有SO2的品红(1分);SO2气体逸出,品红溶液恢复红色(2分)
II(1)稀氨水和酚酞(1分);稀氨水中的NH3逸出,碱性减弱,所以溶液的颜色变浅(2分);(2)溶有SO2的品红(1分);SO2气体逸出,品红溶液恢复红色(2分)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目