题目内容
下列反应的离子方程式正确的是 ( )
A.苯酚钠溶液中通入少量二氧化碳: |
| B.等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合: Ca2++ 2HCO3- + 2OH- = CaCO3↓+ CO32- + 2H2O |
| C.碳酸锌溶于稀硝酸中:CO32-+ 2H+= H2O + CO2↑ |
| D.少量Cl2通入KI溶液中:Cl2+ 2I- = 2C1- + I2 |
D
A:苯酚钠与CO2的产物只能是碳酸氢盐,不正确
B:两者的物质的量相同,NaOH不足:Ca2++HCO3-+OH- = CaCO3↓+2H2O,不正确
C:碳酸锌不溶于水,不能拆为离子,不正确
D:正确
B:两者的物质的量相同,NaOH不足:Ca2++HCO3-+OH- = CaCO3↓+2H2O,不正确
C:碳酸锌不溶于水,不能拆为离子,不正确
D:正确

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
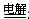 2Cu + O2↑+ 4H+
2Cu + O2↑+ 4H+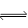 HNO2+OH-
HNO2+OH-