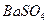题目内容
(1)在BaCl2溶液中滴加Na2C2O4(草酸钠)溶液,产生白色沉淀。在白色沉淀中加入盐酸,沉淀溶解。
①试写出有关反应的离子方程式
②根据上述判断,可得出酸跟盐反应的一种规律是
(2)常温下,0.10 mol/L NH4Cl溶液pH______7(填>、=或<),溶液中各离子浓度由大到小的顺序是______________________________。
(3) Na2S溶液呈碱性的原因是________________________________(写出有关的离子方程式,下同),Al2(SO4)3溶液呈酸性的原因是_______________________________,普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是________________________。
①试写出有关反应的离子方程式
②根据上述判断,可得出酸跟盐反应的一种规律是
(2)常温下,0.10 mol/L NH4Cl溶液pH______7(填>、=或<),溶液中各离子浓度由大到小的顺序是______________________________。
(3) Na2S溶液呈碱性的原因是________________________________(写出有关的离子方程式,下同),Al2(SO4)3溶液呈酸性的原因是_______________________________,普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是________________________。
(1) ①Ba2++C2O2-4=BaC2O4↓ BaC2O4+2H+=Ba2++H2C2O4,
②强酸跟弱酸的盐发生复分解反应,生成弱酸.
(2) < c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(3)
②强酸跟弱酸的盐发生复分解反应,生成弱酸.
(2) < c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(3)

(1)①有关反应的离子方程式:Ba2++C2O42-=BaC2O4↓,BaC2O4+2H+=Ba2++H2C2O4
②根据上述判断,可得出酸跟盐反应的一种规律是:强酸跟弱酸的盐发生复分解反应,生成弱酸
(3) Na2S溶液呈碱性的原因是硫离子水解 S2-+H2O HS-+OH-
HS-+OH-
Al2(SO4)3溶液呈酸性的原因是铝离子水解Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
泡沫灭火器反应原理:3HCO3-+Al3+=3CO2↑+Al(OH)3↓
②根据上述判断,可得出酸跟盐反应的一种规律是:强酸跟弱酸的盐发生复分解反应,生成弱酸
(3) Na2S溶液呈碱性的原因是硫离子水解 S2-+H2O
 HS-+OH-
HS-+OH-Al2(SO4)3溶液呈酸性的原因是铝离子水解Al3++3H2O
 Al(OH)3+3H+
Al(OH)3+3H+泡沫灭火器反应原理:3HCO3-+Al3+=3CO2↑+Al(OH)3↓

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目

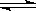 SO2-3+H3O+
SO2-3+H3O+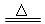 Fe(OH)3↓+3H+
Fe(OH)3↓+3H+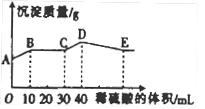
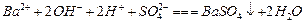
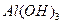 、
、