题目内容
【题目】下列各组微粒,在溶液中能大量共存的是( )
A.Ca2+、Cl﹣、CO32﹣、K+
B.Cu2+、Cl﹣、SO42﹣、OH﹣
C.K+、Cl﹣、NO3﹣、H+
D.H +、Cl﹣、CO32﹣、Na+
【答案】C
【解析】A.Ca2+、CO32﹣结合生成沉淀,不能共存,故A不符合题意;
B.Cu2+、OH﹣结合生成沉淀,不能共存,故B不符合题意;
C.该组离子之间不反应,可大量共存,故C符合题意;
D.H +、CO32﹣结合生成气体和水,不能共存,故D不符合题意;
故答案为:C.
根据离子组中各离子间能否发生离子反应进行判断是否共存即可.

【题目】四种短周期元素在周期表中的相对位置如下表所示,其中Z原子最外层电子数是其电子层数的2 倍。元素M与Z同周期,且原子半径是同周期中最大的。元素R是第四周期的过渡元素;R有甲、乙两种常见氢氧化物,其中甲在常温下置于空气中,会由白色变为灰绿色,最后变为红褐色的乙。
X | Y | |
Z | W |
请按要求回答下列问题:
(1)X的单质的电子式:_________;W最高价氧化物的水化物的化学式:________________。
(2)M、Z、W分别形成的简单离子的半径由大到小顺序为(填离子符号)__________;写一个能说明元素W比元素Z的非金属性强的化学方程式:____________________。
(3)甲变为乙的化学方程式为_______________________。
(4)常温下,当用200mL 1mol·L-1的MOH溶液吸收4.48L(已折算为标准状况)ZY2时,所得溶液的主要溶质(填化学式)为___________;此时溶液pH<7,则其中含Z元素的几种粒子(忽略ZY2)的浓度由大到小的顺序为___________________________。
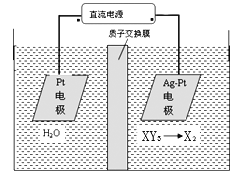
(5) 工业上用电化学法治理酸性废液中的XY3-的原理如图示,其阴极的反应式为_______________。