题目内容
某校甲、乙、丙三个化学兴趣小组利用课外活动时间,设计了不同的课题分别进行了实验探究活动:(1)甲小组进行中和滴定实验,实验室里提供了下面几种仪器:酸式滴定管、碱式滴定管、量筒、托盘天平、普通漏斗、玻璃棒、烧杯,你认为还缺少的玻璃仪器是__________。
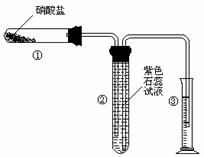
(2)乙小组设计了如下图所示的一套实验装置,以探究该装置的多功能性。

①李明同学认为该装置可以用来制取、收集SO2气体,其中Ⅲ中盛有NaOH溶液。乙小组同学经过讨论后认为该装置存在安全隐患,需要将Ⅲ进行改装,请将改装后的装置图画在方框内。
②王强同学认为可利用该装置快速制取、净化、收集氨气。其中Ⅱ中盛有浓硫酸。你认为是否正确,若正确则不需作答;若不正确,提出改进意见___________________。
(3)丙小组进入了一家回收含铜电缆废料的工厂做社会调查,技术员向同学们展示了两个处理方案,并向同学们提出下列问题:
方案1:

方案2:

①你认为方案___________________更符合当前绿色生产的理念。
②写出方案1中步骤Ⅱ反应的离子方程式__________________。
③技术员指出,无论是方案1还是方案2,都应加入稍过量的铁屑并最终除去,请你设计出去铁屑的操作方法______________________________________________________。
④为了增加经济效益,该工厂把最后一步所得浅绿色溶液,通过__________________、冷却结晶、过滤、洗涤、自然干燥得到一种俗称“绿矾”的工业产品。
⑤丙组同学经查询资料、研究、讨论,又设计了方案3,即把方案2中“加入足量稀硫酸、通入空气并加热”改为“加入足量稀硫酸和H2O
(1)锥形瓶
(2)① (其他合理答案即可)
(其他合理答案即可)
②Ⅱ应该为盛有碱石灰的干燥管或U形管,Ⅲ应改为向下排空气法
(3)①2
②CuO+2H+![]() Cu2++H2O
Cu2++H2O
③将所得红色粉末用稀盐酸或稀硫酸浸泡后,再过滤、洗涤、干燥
④蒸发浓缩
⑤Cu+H2O2+H2SO4![]() CuSO4+2H2O
CuSO4+2H2O
解析:(2)SO2在NaOH溶液中的溶解度较大,应采用防倒吸装置。
②氨气与浓硫酸反应 Ⅱ应为盛有碱石灰的干燥管或U形管,Ⅲ改为向下排空气法。
(3)①方案2更合理;
②CuO+2H+![]() Cu2++H2O;
Cu2++H2O;
③将所得红色粉末用稀盐酸或稀硫酸溶解,再过滤、洗涤、干燥。

 程中气泡部分消失,剩余的气体也能使带火星的木条复燃。石蕊试液也逐渐变为红色,有少量液体被压至装置③中。装置①中的固体逐渐变为黑色。丙同学据此写出了AgNO3受热分解可能的两种化学方程式:学科
程中气泡部分消失,剩余的气体也能使带火星的木条复燃。石蕊试液也逐渐变为红色,有少量液体被压至装置③中。装置①中的固体逐渐变为黑色。丙同学据此写出了AgNO3受热分解可能的两种化学方程式:学科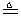 (Ⅰ)4AgNO3 2Ag2O+4NO2↑+O2↑,
(Ⅰ)4AgNO3 2Ag2O+4NO2↑+O2↑,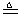 (Ⅰ)4AgNO3
2Ag2O+4NO2↑+O2↑,
(Ⅰ)4AgNO3
2Ag2O+4NO2↑+O2↑,