题目内容
【题目】下列说法中正确的是( )
A.凡是放热反应都是自发的,凡是吸热反应都是非自发的
B.自发反应熵一定增大,非自发反应熵一定减小或不变
C.要判断反应进行的方向,必须综合考虑体系的焓变和熵变
D.自发反应在任何条件下都能实现
【答案】C
【解析】解:A、放热反应有利于反应的自发进行,但是不一定所有的放热反应都是自发反应,故A错误;
B、熵增大的反应有利于反应的自发进行,但是熵增加的反应不一定都是自发反应,故B错误;
C、化学反应能否自发进行的判据是:△H﹣T△S<0,必须综合考虑体系的焓变和熵变,故C正确;
D、过程的自发性仅能用于判断过程的方向,不能确定过程是否一定能发生,故D错误.
故选C.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】含氮化合物在工农业生产中有重要作用。
(1)氨和N2H4是两种常见的氮氢化合物。已知:
4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g)△H1=-541.8kJ·mol-1
2N2(g)+6H2O(g)△H1=-541.8kJ·mol-1
N2H4(g)+O2(g)![]() N2(g)+2H2O(g)△H2=-534kJ·mol-1
N2(g)+2H2O(g)△H2=-534kJ·mol-1
则NH3(g)和O2(g)制取N2H4(g)的热化学方程式为_______________
(2)二氧化氮在一定条件下能发生如下反应:
NO2(g)+SO2(g)![]() SO3(g)+NO(g) △H=-42kJ·mol-1
SO3(g)+NO(g) △H=-42kJ·mol-1
在体积为2L的恒容密闭容器中充入SO2(g)和NO2(g),实验所得数据如下:
实验编号 | 温度 | 起始物质的量/mol | 平衡时物质的量/mol | |
n(SO2) | n(NO2) | n(NO) | ||
甲 | T1 | 4 | 2 | 0.8 |
乙 | T2 | 2 | 4 | 0.6 |
丙 | T1 | 2 | 1 | a |
①在实验甲中,若2min时测得放出的热量是8.4kJ,该温度下的平衡常数为_______(保留到小数点后两位)
②由表中数据可推知T1_____T2(填“﹥“<”或“=”)
③实验丙中,达到平衡时NO2的转化率为_______
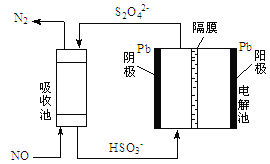
(3)使用间接电化学法可以处理煤烟气中的NO,反应原理如下图所示,已知电解池溶液的pH在4-7之间,写出阴极的电极反应式____________________。