题目内容
某温度下,炭和水蒸汽在密闭容器中发生下列反应: C(s)+H2O(g) 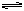 CO(g)+H2(g), CO(g)+H2O(g)
CO(g)+H2(g), CO(g)+H2O(g) 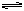 CO2(g)+H2(g) 当反应达平衡时,测得[H2]=1.9mol/L,[CO2]=0.9mol/L,则CO的浓度为( )
CO2(g)+H2(g) 当反应达平衡时,测得[H2]=1.9mol/L,[CO2]=0.9mol/L,则CO的浓度为( )
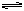 CO(g)+H2(g), CO(g)+H2O(g)
CO(g)+H2(g), CO(g)+H2O(g) 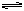 CO2(g)+H2(g) 当反应达平衡时,测得[H2]=1.9mol/L,[CO2]=0.9mol/L,则CO的浓度为( )
CO2(g)+H2(g) 当反应达平衡时,测得[H2]=1.9mol/L,[CO2]=0.9mol/L,则CO的浓度为( )| A.0.1mol/L | B.0.9mol/L | C.1.8mol/L | D.1.9mol/L |
A
根据方程式可知,生成0.9mol/LCO2,则同时消耗CO是0.9mol/L,生成氢气也是0.9mol/L。所以在反应C(s)+H2O(g) 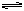 CO(g)+H2(g)中生成的氢气是1.9mol/L-0.9mol/L=1.0mol/L,因此生成的CO也是1.0mol/L,所以最终的CO是1.0mol/L-0.9mol/L=0.1mol/L,答案选A。
CO(g)+H2(g)中生成的氢气是1.9mol/L-0.9mol/L=1.0mol/L,因此生成的CO也是1.0mol/L,所以最终的CO是1.0mol/L-0.9mol/L=0.1mol/L,答案选A。
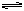 CO(g)+H2(g)中生成的氢气是1.9mol/L-0.9mol/L=1.0mol/L,因此生成的CO也是1.0mol/L,所以最终的CO是1.0mol/L-0.9mol/L=0.1mol/L,答案选A。
CO(g)+H2(g)中生成的氢气是1.9mol/L-0.9mol/L=1.0mol/L,因此生成的CO也是1.0mol/L,所以最终的CO是1.0mol/L-0.9mol/L=0.1mol/L,答案选A。
练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
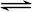 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是( )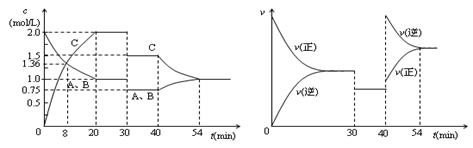
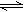 2Z(g)达到平衡时有50%的Y转化为气体Z,若X的转化率为25%,则起始时充入容器的X与Y的物质的量之比应为( )
2Z(g)达到平衡时有50%的Y转化为气体Z,若X的转化率为25%,则起始时充入容器的X与Y的物质的量之比应为( ) CO2(气)+NO(气)△H<0,达到平衡后,只改变其中一个条件,对平衡的影响是:
CO2(气)+NO(气)△H<0,达到平衡后,只改变其中一个条件,对平衡的影响是:
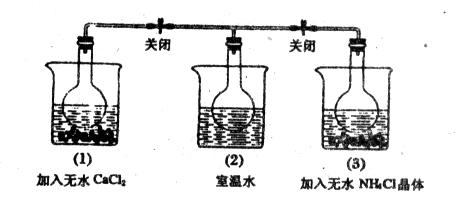
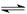 H2(g)+I2(g);△H>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是
H2(g)+I2(g);△H>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是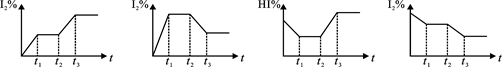
 3C(g)+D(g),达到平衡时C的浓度为W mol·L-1。若维持容器体积和温度不变,按下列四种方法改变起始物质及其量,达到平衡后C的浓度仍为W mol·L-1的是( )
3C(g)+D(g),达到平衡时C的浓度为W mol·L-1。若维持容器体积和温度不变,按下列四种方法改变起始物质及其量,达到平衡后C的浓度仍为W mol·L-1的是( ) 2C(g)若经2s 后测得C的浓度为0.6mol?L-1现有下列几种说法其中不正确的是
2C(g)若经2s 后测得C的浓度为0.6mol?L-1现有下列几种说法其中不正确的是