题目内容
取含MnO2的软锰矿石27.86g,跟足量浓盐酸反应,制得5.6L氯气(该状态下Cl2密度为3.17g/L)计算:
(1)这种软锰矿石中MnO2的质量分数?
(2)被氧化的HCl为多少g?
(1)这种软锰矿石中MnO2的质量分数?
(2)被氧化的HCl为多少g?
(1)78.1% (2)18.25
试题分析:解:(1)设该27.86g含有的MnO2的质量为x,被氧化的HCl的质量为y,根据
MnO2 + 4HCl(浓) = MnCl2 + Cl2↑
87 146 71
x y 3.17×5.6=17.752g
即
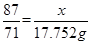 ,解得
,解得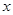 =21.752,
=21.752,所以这种软锰矿石中MnO2的质量分数=21.752/27.86×100%="78.1%" ;
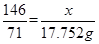 解得y=36.50g,即参加反应的HCl为36.50g,
解得y=36.50g,即参加反应的HCl为36.50g,即被氧化的HCl=1/2×36.50=18.25g。
点评:本题考查了化学反应方程式的简单计算,该题难度适中,但是要注意5.6L的氯气并不是在标准状况下的。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是 2HCOOH+O2,下列说法正确的是
2HCOOH+O2,下列说法正确的是 2Na2S+Na2SO3+3H2O。反应中氧化剂和还原剂的质量比为( )
2Na2S+Na2SO3+3H2O。反应中氧化剂和还原剂的质量比为( ) 加热可发生如下分解:
加热可发生如下分解: (未配平),将气体产物收集于试管中并倒扣于盛)水的水槽中,气体全部被吸收,水充满试管。则生成的铀的氧化物化学式是
(未配平),将气体产物收集于试管中并倒扣于盛)水的水槽中,气体全部被吸收,水充满试管。则生成的铀的氧化物化学式是


