题目内容
已知:2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O;Cl2+2FeCl2===2FeCl3;
2KI+2FeCl3===2KCl+I2+2FeCl2。则下列判断错误的是
2KI+2FeCl3===2KCl+I2+2FeCl2。则下列判断错误的是
A.氧化性:MnO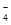 >Cl2>Fe3+ >I2 >Cl2>Fe3+ >I2 |
| B.FeCl3既有氧化性又有还原性 |
| C.向FeI2溶液中通入少量的Cl2,发生反应的方程式为6FeI2+3Cl2=2FeCl3+4FeI3 |
| D.FeCl3能使湿润的淀粉碘化钾试纸变蓝 |
C
试题分析:在氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,所以根据第一个反应可知氧化性:MnO
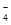 >Cl2,根据第二个反应可确定氧化性:Cl2>Fe3+;根据第三个反应可确定:Fe3+ >I2。所以氧化性由强到弱的顺序是MnO
>Cl2,根据第二个反应可确定氧化性:Cl2>Fe3+;根据第三个反应可确定:Fe3+ >I2。所以氧化性由强到弱的顺序是MnO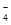 >Cl2>Fe3+ >I2。正确。B.在FeCl3中Fe的化合价为+3价,是该元素的最高化合价,表现氧化性,而Cl元素为其最低化合价,表现还原性,因此FeCl3既有氧化性又有还原性。正确;C.向FeI2溶液中通入少量的Cl2,发生反应的方程式为2I-+Cl2=2Cl-+I2,错误;D.FeCl3能把KI氧化为I2,所以使湿润的淀粉碘化钾试纸变蓝,正确。
>Cl2>Fe3+ >I2。正确。B.在FeCl3中Fe的化合价为+3价,是该元素的最高化合价,表现氧化性,而Cl元素为其最低化合价,表现还原性,因此FeCl3既有氧化性又有还原性。正确;C.向FeI2溶液中通入少量的Cl2,发生反应的方程式为2I-+Cl2=2Cl-+I2,错误;D.FeCl3能把KI氧化为I2,所以使湿润的淀粉碘化钾试纸变蓝,正确。
练习册系列答案
相关题目



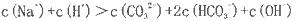
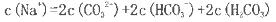
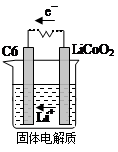
 CoO2+LiC6。则放电时,电池的正极反应式为________________,如图表示该装置工作时电子和离子的移动方向,此时该电池处于_________(填“放电”或“充电”)状态。
CoO2+LiC6。则放电时,电池的正极反应式为________________,如图表示该装置工作时电子和离子的移动方向,此时该电池处于_________(填“放电”或“充电”)状态。