题目内容
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.(1)NO2可用水吸收,相应的化学反应方程式为
3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
.利用反应6NO2+8NH3| 催化剂 |
| 加热 |
6.72
6.72
L.(2)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1
则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=
-41.8
-41.8
kJ?mol-1.一定条件下,将NO2与SO2以物质的量比1:2置于密闭容器中发生上述反应,当反应达到平衡状态时,测得NO2与SO2物质的量比为1:6,则平衡常数K=
| 8 |
| 3 |
| 8 |
| 3 |
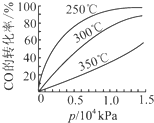
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如下图所示.该反应△H
<
<
0(填“>”或“<”).实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失
在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失
.分析:(1)根据物质与水的反应物与生成物来书写化学反应方程式,再利用氧化还原反应中电子转移计算,然后计算标准状况下气体的体积;
(2)利用盖斯定律来计算反应热,利用三段法计算平衡时的浓度来计算化学平衡常数;
(3)利用化学平衡的影响因素和工业生产的关系来分析.
(2)利用盖斯定律来计算反应热,利用三段法计算平衡时的浓度来计算化学平衡常数;
(3)利用化学平衡的影响因素和工业生产的关系来分析.
解答:解:(1)NO2与H2O反应的方程式为:3NO2+H2O═2HNO3+NO;6NO2+8NH3═7N2+12H2O,当反应中有1 mol NO2参加反应时,共转移了4 mol电子,故转移1.2mol电子时,消耗的NO2为1.2÷4×22.4L=6.72L.
(2)根据盖斯定律,将第二个方程式颠倒过来,与第一个方程式相加得:2NO2+2SO2═2SO3+2NO,△H=-83.6 kJ?mol-1,故NO2+SO2?SO3+NO,△H=-41.8 kJ?mol-1;
设加入的二氧化氮的物质的量为a,则二氧化硫的为2a,
NO2(g)+SO2(g)?SO3(g)+NO(g)
起始物质的量 1a 2a 0 0
转化物质的量 x x x x
平衡物质的量 a-x 2a-x x x
则(a-x):(2a-x)=1:6,x=
,则平衡时,C( NO2)=
mol/L=
mol/L,C(SO2)=
mol/L=
mol/L
C(SO3)=C(NO)=
mol/L,平衡常数K=
=
,故答案为:
;
(3)由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸热反应,正反应是放热反应,△H<0;压强大,有利于加快反应速率,有利于使平衡正向移动,但压强过大,需要的动力大,对设备的要求也高,故选择250℃、1.3×104kPa左右的条件.因为在250℃、压强为1.3×104 kPa时,CO的转化率已较大,再增大压强,CO的转化率变化不大,没有必要再增大压强.
故答案为:<,在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失.
(2)根据盖斯定律,将第二个方程式颠倒过来,与第一个方程式相加得:2NO2+2SO2═2SO3+2NO,△H=-83.6 kJ?mol-1,故NO2+SO2?SO3+NO,△H=-41.8 kJ?mol-1;
设加入的二氧化氮的物质的量为a,则二氧化硫的为2a,
NO2(g)+SO2(g)?SO3(g)+NO(g)
起始物质的量 1a 2a 0 0
转化物质的量 x x x x
平衡物质的量 a-x 2a-x x x
则(a-x):(2a-x)=1:6,x=
| 4a |
| 5 |
| a-x |
| V |
| a |
| 5V |
| 2a-x |
| V |
| 6a |
| 5V |
C(SO3)=C(NO)=
| 4a |
| 5V |
| ||||
|
| 8 |
| 3 |
| 8 |
| 3 |
(3)由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸热反应,正反应是放热反应,△H<0;压强大,有利于加快反应速率,有利于使平衡正向移动,但压强过大,需要的动力大,对设备的要求也高,故选择250℃、1.3×104kPa左右的条件.因为在250℃、压强为1.3×104 kPa时,CO的转化率已较大,再增大压强,CO的转化率变化不大,没有必要再增大压强.
故答案为:<,在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失.
点评:该题将元素化合物与能量变化、化学平衡等知识柔和在一起进行考察,充分体现了高考的综合性,第(3)容易出错,需认真分析图象,注意图象的变化趋势及纵横坐标的含义,从而得出正确结论.

练习册系列答案
相关题目
 (2011?山东)研究NO2、SO2、CO等大气污染气体的处理有重要意义.
(2011?山东)研究NO2、SO2、CO等大气污染气体的处理有重要意义.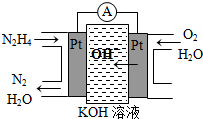 Ⅰ.肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题
Ⅰ.肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题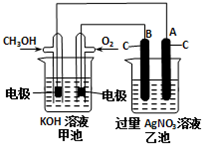 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.