题目内容
6.已知下列反应的热化学方程式如下:CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g)△H1=218.4kJ•mol-1(反应Ⅰ);CaSO4(s)+4CO(g)?CaS(s)+4CO2(g)△H2=-175.6kJ•mol-1(反应Ⅱ).假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是( )| A. |  | B. |  | ||
| C. |  | D. | 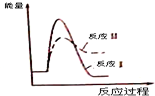 |
分析 反应Ⅰ为吸热反应,反应Ⅱ为放热反应,结合反应物与生成物总能量大小之间的关系判断.
解答 解;反应Ⅰ为吸热反应,反应Ⅱ为放热反应,则A、D错误,因为两图中生成物总能量高于反应物总能量,由题意知:反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则反应Ⅱ的活化能较大,则B错误、C正确,故选C.
点评 本题涉及化学平衡以及反应热与焓变的考查,题目难度中等.

练习册系列答案
相关题目
16. 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电后,发现左侧溶液变蓝色,一段时间后,蓝色又逐渐变浅.(已知:3I2+6OH-═IO3-+5I-+3H2O,IO3-离子无色);下列说法不正确的是( )
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电后,发现左侧溶液变蓝色,一段时间后,蓝色又逐渐变浅.(已知:3I2+6OH-═IO3-+5I-+3H2O,IO3-离子无色);下列说法不正确的是( )
 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电后,发现左侧溶液变蓝色,一段时间后,蓝色又逐渐变浅.(已知:3I2+6OH-═IO3-+5I-+3H2O,IO3-离子无色);下列说法不正确的是( )
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电后,发现左侧溶液变蓝色,一段时间后,蓝色又逐渐变浅.(已知:3I2+6OH-═IO3-+5I-+3H2O,IO3-离子无色);下列说法不正确的是( )| A. | 右侧发生的电极反应式:2H2O+2e-═H2↑+2OH- | |
| B. | a为电源正极 | |
| C. | 电解结束时,右侧溶液中没有IO3- | |
| D. | 用阴离子交换膜,电解槽内发生的总化学方程式为:KI+3H2O$\frac{\underline{\;电解\;}}{\;}$ KIO3+3H2↑ |
17.类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其是否正确.下列几种类推结论中正确的是( )
| A. | 由2Cu+O2$\frac{\underline{\;△\;}}{\;}$2CuO可推出同族的硫也有Cu+S$\frac{\underline{\;△\;}}{\;}$CuS | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | Na能与水反应生成H2,K、Ca也能与水反应生成H2 | |
| D. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
14.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 等物质的量的N2和CO所含分子数均为NA | |
| B. | 1.7 g H2O2中含有的电子数为0.9NA | |
| C. | 标准状况下,22.4L空气含有NA个单质分子 | |
| D. | 1mol•L-1NaCl溶液含有NA个Na+ |
1.H7N9型禽流感是全球首次发现的新亚型流感病毒,达菲(Tamiflu)是治疗该病毒的最佳药物.以莽草酸为原料,经多步反应可制得达菲和对羟基苯甲酸.达菲、莽草酸、对羟基苯甲酸的结构简式如图:

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 达菲的分子式为C16H30N2PO8 | |
| B. | 达菲、莽草酸、对羟基苯甲酸都属于芳香族化合物 | |
| C. | 利用FeCl3溶液可区别莽草酸和对羟基苯甲酸 | |
| D. | 1mol莽草酸与NaOH溶液反应,最多消耗4mol NaOH |
11.实验室中需要配制1mol/L的NaCl溶液970mL,配制时应选用的容量瓶的规格是( )
| A. | 950mL 容量瓶 | B. | 500mL容量瓶 | ||
| C. | 1000mL 容量瓶 | D. | 任意规格的容量瓶 |
15.木炭、氧化铜和铁粉都是黑色粉末,用化学方法鉴别它们最理想的试剂是下列物质中的( )
| A. | 稀硫酸 | B. | 硫酸铜溶液 | C. | 氢氧化钠溶液 | D. | 水溶解度/gA |
16.下列反应的离子方程式书写正确的是( )
| A. | 电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 向AlCl3溶液中加入过量的氨水:Al3++4NH3.H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| C. | Cu与浓硝酸反应制备N02:3Cu+8H++2NO${\;}_{3}^{-}$═3Cu2++2NO2↑+4H2O | |
| D. | 向KAl(S04)2溶液中滴加Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO${\;}_{4}^{2-}$+2Ba2++4OH-═AlO${\;}_{2}^{-}$+2BaSO4↓+2H2O |
 已知2NO2(g)═N2O4(g)△H(298K)=-52.7kJ•mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
已知2NO2(g)═N2O4(g)△H(298K)=-52.7kJ•mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验: