题目内容
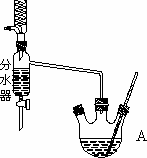
下图为制取乙酸乙酯的实验装置图。回答下列问题:

(1)揭示实验原理
①乙酸与乙醇在催化剂存在的条件下加热可以发生反应生成乙酸乙酯。请用氧同位素示踪法写出乙酸与乙醇发生酯化反应的化学方程式______________________。
②能否用氢同位素示踪法揭示酯化反应原理? _______(选填“能”或“不能”),原因是___________________。
(2)反应温度确定:
合成乙酸乙酯的反应为放热反应。实验表明,反应温度应控制在85℃左右为宜。回答:
实验温度不宜低于85℃左右的原因是__________________________________________;
实验温度不宜高于85℃左右的原因是__________________________________________;
(3)实验装置的比较:
利用如图装置制备乙酸乙酯,这种装置与教材装置相比较突出的优点是__________________________。
(4)酯层厚度的标示:
为更好地测定酯层厚度,可预先向饱和Na2CO3溶液中滴加1滴____试液,现象是____________________________。
(1)① (2分)
(2分)
②否。醇和羧酸都失H,所以H换成D无法指示何种物质脱羟基。(各1分,共2分)
(2)反应速率低,达不到催化剂活性温度;温度过高利于平衡逆向移动,酯产率降低。(各2分,共4分)
(3)用分水器能够在反应进行时很容易的把水分离出来,从而使平衡正向移动,提高乙酸乙酯的产率。(合理即给分 2分)
(4)酚酞。碳酸钠层呈红色,上层的酯层呈无色。(各1分,共2分)
【解析】
试题分析:
(1)酯化反应中羧酸提供羟基,醇应该氢原子,所以反应的机理可以表示为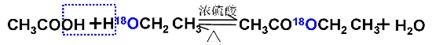 。
。
(2)由于醇和羧酸都失H,所以H换成D无法指示何种物质脱羟基,因此不能用氢同位素示踪法揭示酯化反应原理。
温度低,反应速率低,且达不到催化剂活性温度,所以温度不能低于85℃;正反应是放热反应,温度过高利于平衡逆向移动,酯产率降低,所以也不能高于85℃。
(3)根据装置图的结构特点可判断,用分水器能够在反应进行时很容易的把水分离出来,从而降低生成物浓度。使平衡正向移动,提高乙酸乙酯的产率。
(4)由于碳酸钠溶液显碱性,能使酚酞试液显红色,所以应该滴入酚酞试液,实验现象是碳酸钠层呈红色,上层的酯层呈无色。
考点:考查酯化反应原理的探究、外界条件对反应速率和平衡对影响以及实验评价

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案 “酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯.
“酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯.