题目内容
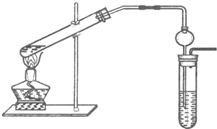
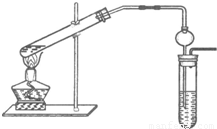
 “酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯.
“酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯.回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式:
CH3COOH+CH3CH2OH
CH3COOC2H5+H2O.
| 浓硫酸 |
| △ |
CH3COOH+CH3CH2OH
CH3COOC2H5+H2O.
| 浓硫酸 |
| △ |
(2)浓硫酸的作用是:①
催化作用
催化作用
;③脱水剂;
脱水剂;
(3)插入右边试管的导气管上接有一个球状容器,其作用为
防止吸收液倒吸入试管;
防止吸收液倒吸入试管;
(4)将接收液与乙酸乙酯分离的方法是
分液;
分液;
(5)做此实验时,有时还向作反应容器的试管里加入几块碎瓷片,其目的是
防止暴沸;
防止暴沸;
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有
①
①
(填序号)①单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
②单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
③混合物中各物质的物质的量相等.
分析:(1)乙酸与乙醇在浓硫酸作用下加热,生成乙酸乙酯;
(2)浓硫酸起到了催化作用和脱水作用;
(3)防止倒吸装置;
(4)乙酸乙酯不溶于水;
(5)液体加热要加碎瓷片,防止暴沸;
(6)达到平衡状态,各种成分的物质的量不再发生变化;
(2)浓硫酸起到了催化作用和脱水作用;
(3)防止倒吸装置;
(4)乙酸乙酯不溶于水;
(5)液体加热要加碎瓷片,防止暴沸;
(6)达到平衡状态,各种成分的物质的量不再发生变化;
解答:解:(1)乙酸乙酯制取的反应方程式是:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O,
故答案是:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O;
(2)、反应中,浓硫酸脱去乙酸中的羟基和乙醇中的氢氧根生成水,同时起到催化作用,故答案是:
①脱水剂,②催化剂;
(3)、乙酸乙酯制备试管受热不均,导管伸入液面下可能发生倒吸,
故答案是:防止吸收液倒吸入试管;
(4)、由于乙酸乙酯不溶于水,可以采用分液方法分离,
故答案是:分液;
(5)、在给液体加热时,加入 碎瓷片可以防止暴沸,
故答案是:防止暴沸;
(6)、处于平衡状态时,同种物质的消耗和生成的相等,各种成分的物质的量不再发生变化,
①单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸,生成1mol乙酸乙酯时,同时消耗了1mol乙酸,所以达到了平衡状态,故①正确;
②无法判断是否达到平衡,故②错误;
③各个物质的物质的量大小无法判断是否平衡,关键看是否发生变化,故③错误.
本题答案的:①.
| 浓硫酸 |
| △ |
故答案是:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
(2)、反应中,浓硫酸脱去乙酸中的羟基和乙醇中的氢氧根生成水,同时起到催化作用,故答案是:
①脱水剂,②催化剂;
(3)、乙酸乙酯制备试管受热不均,导管伸入液面下可能发生倒吸,
故答案是:防止吸收液倒吸入试管;
(4)、由于乙酸乙酯不溶于水,可以采用分液方法分离,
故答案是:分液;
(5)、在给液体加热时,加入 碎瓷片可以防止暴沸,
故答案是:防止暴沸;
(6)、处于平衡状态时,同种物质的消耗和生成的相等,各种成分的物质的量不再发生变化,
①单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸,生成1mol乙酸乙酯时,同时消耗了1mol乙酸,所以达到了平衡状态,故①正确;
②无法判断是否达到平衡,故②错误;
③各个物质的物质的量大小无法判断是否平衡,关键看是否发生变化,故③错误.
本题答案的:①.
点评:本题考查乙酸乙酯的制取,是基础性试题的考查,难度不大,主要是考查学生对乙酸乙酯制备原理的熟悉了解程度,意在培养学生分析、归纳、总结问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(1)某同学为探究蔗糖的水解反应,进行如下实验,填写实验步骤III的实验现象:
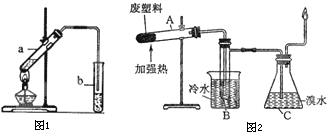
(2)“酒是陈的香”的原因之一是储存过程中生成了有香味的酯.实验室用下图所示装置制取乙酸乙酯.
①试管a中生成乙酸乙酯的化学反应方程式是 .
②试管b中盛放的试剂是 溶液
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是 .
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) .
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
实验装置如图所示.
①试管A中的最终残余物为 ;
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有 种.
③锥形瓶C中观察到的现象是 ;经溴水充分吸收再干燥后,剩余两种气体的平均相对分子质量为 .

| 实验步骤 | 实验现象 |
| I.向编号为①②③的3支试管中,分别加入1mL 20%的蔗糖溶液,向试管②和③中加入0.5mL稀硫酸,并将这3支试管同时水浴加热约5min | 均无明显现象 |
| II.取试管①和②,加入新制氢氧化铜悬浊液,加热至沸腾 | 均无明显现象 |
| III.取试管③,先加入NaOH溶液调溶液pH至碱性,再加入新制氢氧化铜悬浊液,加热至沸腾 | |
| 结论:证明蔗糖在稀硫酸作用下发生了水解反应 | |
①试管a中生成乙酸乙酯的化学反应方程式是
②试管b中盛放的试剂是
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
①试管A中的最终残余物为
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有
③锥形瓶C中观察到的现象是
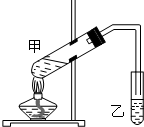 (1)“酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图装置制取乙酸乙酯.
(1)“酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图装置制取乙酸乙酯.