题目内容
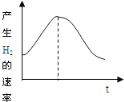
【题目】把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速率的主要因素是
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A. ①④ B. ③④ C. ①③ D. ②③
【答案】C
【解析】
由图可知,该反应速率先增大后减小,结合温度、浓度对反应速率的影响解答。
由图可知,该反应速率先增大后减小,该反应为放热反应,放出热量,温度升高,则反应速率加快,后来盐酸浓度减小,则反应速率逐渐减小,即前一阶段温度对反应速率的影响其主要作用,后一阶段浓度对反应速率的影响起主要作用。因Cl-不参加反应,Cl-的浓度增大或减小都不影响化学反应速率,且该反应中Cl-的浓度可视为不变,另外镁条的表面积会影响反应速率,但在该反应中不是主要因素,即影响因素主要为①③,答案选C。

练习册系列答案
相关题目
【题目】下图为元素周期表的一部分,根据元素a~j在周期表中的位置,按要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | a | |||||||
2 | b | c | d | e | ||||
3 | f | g | h | i | j | |||
(1)在a ~j中,化学性质最不活泼的元素是___________(填元素符号)。
(2)f、g、h的单质分别与水反应,最剧烈的是___________(填元素符号)。
(3)c、i的氢化物稳定性较强的是____________(填化学式)。
(4)c、f可形成既含离子键又含非极性键的化合物,该化合物的电子式为__________。
(5)d、f、g的离子半径最大的是_______________(填离子符号)。
(6)f的最高价氧化物的水化物与h的最高价氧化物的水化物反应的离子方程式为:___________________________________。