题目内容
8.下列化合物中,只含有共价键的是( )| A. | H2O | B. | CaCl2 | C. | NaCl | D. | NaOH |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,以此来解答.
解答 解:A.只含H-O共价键,故A选;
B.只含钙离子与氯离子之间的离子键,故B不选;
C.只含钠离子与氯离子之间的离子键,故C不选;
D.含钠离子与氢氧根离子之间的离子键和O-H共价键,故D不选;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意特殊物质中的化学键,题目难度不大.

练习册系列答案
相关题目
10.化学与人类生活密切相关,下列说法正确的是( )
| A. | 硅胶可用作食品干燥剂 | |
| B. | 氢氧化铝和氢氧化钠都是常见的胃酸中和剂 | |
| C. | 生活中使用的合成纤维和光导纤维都是有机物 | |
| D. | PM2.5中含有的铅、镉、砷等有害元素都是金属元素 |
11.丙烯酸的结构简式为CH2=CH-COOH,其对应的性质中错误的是( )
| A. | 能与钠反应放出氢气 | B. | 能与新制的Cu(OH)2悬浊液反应 | ||
| C. | 能与溴水发生取代反应 | D. | 能和HBr发生加成反应 |
8.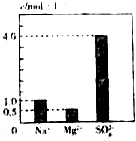 0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )
0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )
 0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )
0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )| A. | 该溶液中NaSO4的物质的量浓度为1.0mol•L-1 | |
| B. | 该溶液中MgSO4的物质的量为0.25mol | |
| C. | 该溶液中MgSO4的质量为30g | |
| D. | 该溶液中Al2(SO4)3的物质的量浓度为1.0mol•L-1 |
3.下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)④⑤⑥的原子半径由小到大的顺序为(用元素符号表示)O<Al<Na.
②③⑦的最高价含氧酸的酸性由弱到强的顺序是(用化学式表示)H2SiO3<H2CO3<HNO3.
(2)写出由以上①④⑤元素构成的化合物的电子式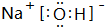 ;该化合物含有的化学键类型有离子键、共价键.
;该化合物含有的化学键类型有离子键、共价键.
(3)⑥的最高价氧化物分别与强酸、强碱反应的离子方程式为Al2O3+6H+=2Al3++3H2O;Al2O3+2OH-=2AlO2-+H2O.
| 周期 族 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
②③⑦的最高价含氧酸的酸性由弱到强的顺序是(用化学式表示)H2SiO3<H2CO3<HNO3.
(2)写出由以上①④⑤元素构成的化合物的电子式
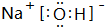 ;该化合物含有的化学键类型有离子键、共价键.
;该化合物含有的化学键类型有离子键、共价键.(3)⑥的最高价氧化物分别与强酸、强碱反应的离子方程式为Al2O3+6H+=2Al3++3H2O;Al2O3+2OH-=2AlO2-+H2O.
20.已知蓝铜矿的主要成分为2CuCO3•Cu(OH)2,用焦炭与蓝铜矿加热可用于工业炼铜,同时产生一种常见的能产生温室效应的气体和一种常见液体.下列叙述不正确的是( )
| A. | 1mol 2CuCO3•Cu(OH)2完全反应转移电子的数目为6NA | |
| B. | 该反应在理论上用1mol焦炭可以还原得到2mol铜 | |
| C. | 该反应的氧化剂与还原剂的物质的量之比为4:3 | |
| D. | 工业炼铜还可以采用以下方法:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2 |
17.下列有关说法正确的是( )
| A. | 在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 | |
| B. | 常温下,PH均为5的盐酸、氯化铵溶液中,水的电离程度相同 | |
| C. | 8NH3(g)+6NO(g)═7N2(g)+12H2O(g)△H<0,则该反应一定能自发进行 | |
| D. | 对于乙酸乙酯的水解反应(△H>0)加入少量氢氧化钠溶液并加热,该反应的反应速率和平衡常数均减小 |
18.下列关于氧化还原反应的说法不正确的是( )
| A. | 氧化还远反应的实质是电子的转移 | |
| B. | 含最高价元素的化合物均具有强氧化性 | |
| C. | 一定存在元素化合价的变化 | |
| D. | 氧化剂和还原剂混合不一定发生氧化还原反应 |
