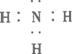题目内容
已知离子化合物A由两种短周期元素组成,且A中阴、阳离子的电子层结构相同。从固体A开始,可以发生如下框图变化,已知Cu2+、Cu(OH)2均能与气体H形成的[Cu(H)4]2+离子在溶液中呈深蓝色。?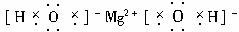 ?
?
(1)在实验室用集气瓶收集气体G和气体H。则收集气体G的方法是 ,检验气体H已收集满的方法是 。?
(2)在实验室进行操作①时,除了使用酒精灯、铁架台、铁圈及夹持仪器外,还缺少的玻璃仪器是 ,在进行操作②时,应在HCl的气氛中加热脱水,其目的是 。?
(3)F位于元素周期表第? ?周期? ?族,写出其最高价氧化物对应的水化物的电子式? ?。写出反应A+H2O→B+H的化学方程式 。?
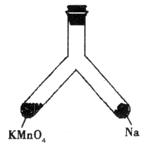
(4)某学生设计如图15-38装置,将产生的气体H通入硫酸铜溶液,制得深蓝色溶液J。现有下列?试剂?:?
 ?
?
图15-38
①稀NaOH溶液 ②H2O2溶液 ?③浓氨水 ?④NH4Cl?溶液 ⑤生石灰 ?⑥消石灰 ⑦碳酸氢钠?
(Ⅰ)a中的试剂:固体X应是? ?(填序号),溶液Y应是 (填序号)。
(Ⅱ)你认为使用装置b时存在的主要缺点: (用简明文字叙述)。?
(1)用向上排空气法(或排饱和食盐水法) 把湿润的红色石蕊试纸粘在玻璃棒上(或用镊子夹取湿润的红色石蕊试纸),靠近集气瓶口,观察试纸颜色变化。若试纸变为蓝色则证明已收集满NH3(其他答案只要合理也可)??
(2)玻璃棒 防止MgCl2在加热时水解?
(3)2 ⅡA?
![]() Mg3N2+6H2O
Mg3N2+6H2O![]() 3Mg(OH)2↓+2NH3↑?
3Mg(OH)2↓+2NH3↑?
(4)(Ⅰ)⑤ ③ (Ⅱ)易发生倒吸?
解析:(1)本题中明显现象(结合信息)是“浅蓝色沉淀I”和“深蓝色溶液J”,由此推出气体H是氨气,黄绿色气体是氯气,所以收集气体G的方法是
用向上排空气法(或排饱和食盐水法),检验气体H收集满的方法是把湿润的红色石蕊试纸粘在玻璃棒上,靠近集气瓶口,观察试纸颜色变化。若试纸变为蓝色则证明已收集满NH3。?
(2)因为操作①是过滤,所以缺少的玻璃仪器为玻璃棒。由A能水解产生氨气,且水解产物不溶于过量的碱溶液,得A是Mg3N2;因MgCl2极易水解,所以进行操作②时要加酸性条件,即防止MgCl2在加热时水解。?
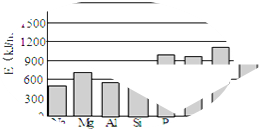
(3)由图可推出F是Mg,位于第2周期ⅡA族,Mg(OH)2电子式为![]() ,Mg3N2水解方程式为:Mg3N2+6H2O
,Mg3N2水解方程式为:Mg3N2+6H2O![]() 3Mg(OH)2↓+2NH3↑
3Mg(OH)2↓+2NH3↑
(4)从图看,该反应不需加热,并且产生的气体应是氨气,所以固体X应是碱,即⑤或⑥,Y应是浓氨水,由于氨气极易溶于水,所以b装置缺点是易发生倒吸。

 名校课堂系列答案
名校课堂系列答案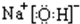
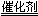 2H2O+O2↑
2H2O+O2↑