题目内容
I.(1)下列有关实验操作或测量数据合理的是___________(填写序号)
a.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8 mL的Na2CO3溶液
d.实验室酸制氯化亚锡溶液时,可以先将氯化亚锡溶解在盐酸中,再配制到所需要的浓度
e.使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤干净
f.在用稀硫酸和锌粒反应制取氢气时加入少许硫酸铜以加快化学反应速率
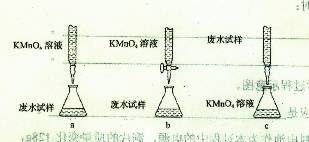
II.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计如图所示实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题。
a.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8 mL的Na2CO3溶液
d.实验室酸制氯化亚锡溶液时,可以先将氯化亚锡溶解在盐酸中,再配制到所需要的浓度
e.使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤干净
f.在用稀硫酸和锌粒反应制取氢气时加入少许硫酸铜以加快化学反应速率
II.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计如图所示实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题。

(2)实验室制备乙烯的化学方程式______________________。升温到140℃时的副反应产物的结构简式
___________。
(3)图中①.②.③.④装置可盛放的试剂是:①___________;②___________;③___________;
④___________。(将下列有关试剂的序号填入空格内)
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(4)能说明二氧化硫气体存在的现象是______________________
(5)使用装置②的目的是_________________________________
(6)使用装置③的目的是_________________________________
(7)确定含有乙烯的现象是_______________________________
___________。
(3)图中①.②.③.④装置可盛放的试剂是:①___________;②___________;③___________;
④___________。(将下列有关试剂的序号填入空格内)
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(4)能说明二氧化硫气体存在的现象是______________________
(5)使用装置②的目的是_________________________________
(6)使用装置③的目的是_________________________________
(7)确定含有乙烯的现象是_______________________________
(1)cdf
(2)CH3CH2OH CH2=CH2↑+H2O;CH3CH2-O-CH2CH3
CH2=CH2↑+H2O;CH3CH2-O-CH2CH3
(3)① A ;② B ;③ A ;④ D 。
(4)装置①中品红溶液褪色
(5)除掉二氧化硫以免干扰乙烯的性质实验
(6)检验二氧化硫是否除尽
(7)③中的溶液褪色,④中的溶液不褪色
(2)CH3CH2OH
 CH2=CH2↑+H2O;CH3CH2-O-CH2CH3
CH2=CH2↑+H2O;CH3CH2-O-CH2CH3 (3)① A ;② B ;③ A ;④ D 。
(4)装置①中品红溶液褪色
(5)除掉二氧化硫以免干扰乙烯的性质实验
(6)检验二氧化硫是否除尽
(7)③中的溶液褪色,④中的溶液不褪色

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目