题目内容
CuSO4溶液与Na2CO3溶液混合产生蓝绿色沉淀,以下是某兴趣小组对沉淀组成的探究。
【提出假设】
假设1:沉淀为Cu (OH)2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3·mCu (OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【定性探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如下装置(夹持仪器未画出)进行定性实验;
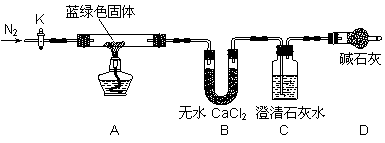 |
(1)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设 成立。
(2)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是 (填代号)。
a.浓硫酸 b.无水CuSO4 c.碱石灰 d.P2O5
(3)乙同学更换B试剂后验证假设3成立的实验现象是 。
【定量探究】
(4)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在20℃的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是 (双选,填代号)
| 溶解度(S)/g | 溶度积(Ksp) | 摩尔质量(M)/g·mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
a.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
b.Ba(OH)2为强碱,Ca(OH)2为弱碱
c.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
d.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为54.2 g,实验结束后装置B的质量增加5.4 g,C中的产生沉淀的质量为39.4 g。则该蓝绿色固体的化学式为 。
CuCO3(1分)
(1)1(1分)
(2)b(2分);
(3)A中蓝绿色固体变黑色,B中无水CuSO4固体变蓝,C中有白色沉淀产生(3分)【A、B、C中每个现象各1分】
(4)①ac(2分)【漏一个得1分,错一个倒扣1分,扣完为止】
②2CuCO3·3Cu(OH)2、或3Cu(OH)2·2CuCO3或Cu5(OH)6(CO3)2(3分)

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案下表选项中对规定反应的离子方程式的评价合理的是
| 选项 | 反应 | 离子方程式 | 评价 |
| A | FeI2和Cl2以5:7的物质的量比反应 | 4Fe2++10I-+7Cl2 =4Fe3++5I2 + 14Cl- | 正确 |
| B | 碳酸氢钠溶液与足量的氢氧化钡溶液反应 | Ba2++ 2OH-+ 2HCO3-=BaCO3↓+ CO32- + 2H2O | 正确 |
| C | 金属Na和CuSO4溶液反应 | Na + Cu2+=Na+ + Cu | 错误。离子方程式不符合电荷守恒原则 |
| D | 过量二氧化碳通入次氯酸钙溶液中反应 | 2C1O-+H2O+CO2 =2HClO + CO32- | 错误。生成物碳酸钙 不应写成离子形式 |
下表选项中对规定反应的离子方程式的评价合理的是
|
选项 |
反应 |
离子方程式 |
评价 |
|
A |
FeI2和Cl2以5:7的物质的量比反应 |
4Fe2++10I-+7Cl2 =4Fe3++5I2 + 14Cl- |
正确 |
|
B |
碳酸氢钠溶液与足量的氢氧化钡溶液反应 |
Ba2++ 2OH-+ 2HCO3-= BaCO3↓+ CO32- + 2H2O |
正确 |
|
C |
金属Na和CuSO4溶液反应 |
Na + Cu2+ = Na+ + Cu |
错误。离子方程式不符合电荷守恒原则 |
|
D |
过量二氧化碳通入次氯酸钙溶液中反应 |
2C1O-+H2O+CO2 =2HClO + CO32-
|
错误。生成物碳酸钙 不应写成离子形式 |