题目内容
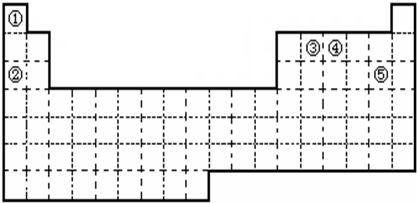
①~⑤五种元素在元素周期表中的位置如图所示:

回答下列问题:
(1)①~⑤五种元素中,非金属性最强的元素在周期表中的位置是 ,;
(2)②③④元素原子中,半径最小的是 (填元素符号);
(3)元素①和③可以形成众成多的化合物,其中最简单的是 (化学式).该化合物中,化学键的类型为 (选填“极性共价键”、“非极性共价键”或“离子键”);
(4)元素⑤单质与水反应的离子方程式: .

回答下列问题:
(1)①~⑤五种元素中,非金属性最强的元素在周期表中的位置是
(2)②③④元素原子中,半径最小的是
(3)元素①和③可以形成众成多的化合物,其中最简单的是
(4)元素⑤单质与水反应的离子方程式:
分析:根据元素在周期表中的位置知,①②③④⑤分别是H、Na、C、N、Cl元素,
(1)同一周期中,元素的非金属性随着原子序数的增大而增强,同一主族中,元素的非金属性随着原子序数的增大而减弱;
(2)同主族自上而下,其原子半径越大,同一周期元素中,元素的原子半径随着原子序数的增大而减小;
(3)元素①和③可以形成众成多的化合物,其中最简单的是甲烷,不同非金属元素之间易形成极性共价键;
(4)氯气和水反应生成盐酸和次氯酸.
(1)同一周期中,元素的非金属性随着原子序数的增大而增强,同一主族中,元素的非金属性随着原子序数的增大而减弱;
(2)同主族自上而下,其原子半径越大,同一周期元素中,元素的原子半径随着原子序数的增大而减小;
(3)元素①和③可以形成众成多的化合物,其中最简单的是甲烷,不同非金属元素之间易形成极性共价键;
(4)氯气和水反应生成盐酸和次氯酸.
解答:解:根据元素在周期表中的位置知,①②③④⑤分别是H、Na、C、N、Cl元素,
(1)同一周期中,元素的非金属性随着原子序数的增大而增强,同一主族中,元素的非金属性随着原子序数的增大而减弱,所以这几种元素中非金属性最强的是Cl元素,Cl元素位于第三周期、第VIIA族,
故答案为:第三周期、第VIIA族;
(2)同主族自上而下,其原子半径越大,同一周期元素中,元素的原子半径随着原子序数的增大而减小,所以②③④元素原子中,原子半径大小顺序是Na>C>N,所以原子半径最小的是N元素,
故答案为:N;
(3)元素①和③可以形成众成多的化合物,其中最简单的是CH4,不同非金属元素之间易形成极性共价键,甲烷中只含极性共价键,
故答案为:CH4;极性共价键;
(4)氯气和水反应生成盐酸和次氯酸,离子反应方程式为:Cl2+H2O=H++Cl-+HClO,
故答案为:Cl2+H2O=H++Cl-+HClO.
(1)同一周期中,元素的非金属性随着原子序数的增大而增强,同一主族中,元素的非金属性随着原子序数的增大而减弱,所以这几种元素中非金属性最强的是Cl元素,Cl元素位于第三周期、第VIIA族,
故答案为:第三周期、第VIIA族;
(2)同主族自上而下,其原子半径越大,同一周期元素中,元素的原子半径随着原子序数的增大而减小,所以②③④元素原子中,原子半径大小顺序是Na>C>N,所以原子半径最小的是N元素,
故答案为:N;
(3)元素①和③可以形成众成多的化合物,其中最简单的是CH4,不同非金属元素之间易形成极性共价键,甲烷中只含极性共价键,
故答案为:CH4;极性共价键;
(4)氯气和水反应生成盐酸和次氯酸,离子反应方程式为:Cl2+H2O=H++Cl-+HClO,
故答案为:Cl2+H2O=H++Cl-+HClO.
点评:本题考查了元素周期表和元素周期律的综合应用,明确元素周期律及其应用是解本题关键,难度不大.

练习册系列答案
相关题目
 A、B、C、D、E五种元素在元素周期表中的位置如图所示:
A、B、C、D、E五种元素在元素周期表中的位置如图所示: