��Ŀ����
����Ŀ��A��B��C��X��Ϊ��ѧ�����Ĵ��������֮��������ת����ϵ����Ӧ����������������ȥ����
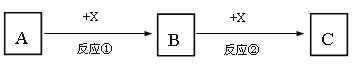
��1����A��B��C��Ϊ����ͬ�ַǽ���Ԫ�صĻ����AΪʹʪ��ĺ�ɫʯ����ֽ���������壬B�Ӵ��������̱�ΪC����Ӧ���Ļ�ѧ����ʽΪ_______________________��
��2����A��B��CΪ��ɫ��Ӧ���ʻ�ɫ�Ļ����XΪ��ɫ��ζ���壬��Ӧ�������ӷ���ʽΪ_____________________________________________��
��3����A��B��C��Ϊ����ͬ�ֽ���Ԫ�صĻ����X��ǿ���Ӧ�������ӷ���ʽΪ________________________________________________��
��4����AΪ����Fe��XΪϡ���ᣬ��Ӧ�������ӷ���ʽΪ___________________������B����Һ�м�������������Һ������Ϊ________________________________________����Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
��5����A��X��Ϊ���ʣ�BΪ��ʹƷ����Һ��ɫ�����壬��Ӧ���Ļ�ѧ����ʽΪ___________________________��
���𰸡� ![]() CO32- + CO2 + H2O �� 2HCO3- Al��OH��3 + OH- �� AlO2- + 2H2O 3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O �Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3
CO32- + CO2 + H2O �� 2HCO3- Al��OH��3 + OH- �� AlO2- + 2H2O 3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O �Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3 ![]()
����������1����A��B��C��Ϊ����ͬ�ַǽ���Ԫ�صĻ����AΪʹʪ��ĺ�ɫʯ����ֽ���������壬A�ⰱ����B�Ӵ��������̱�ΪC��BΪNO��CΪNO2����Ӧ���Ļ�ѧ����ʽΪ![]() ����2����A��B��CΪ��ɫ��Ӧ���ʻ�ɫ�Ļ����A��B��C�ֱ�ΪNa2O2 ��Na2O ��Na2CO3��NaHCO3��XΪ��ɫ��ζ���壬XΪCO2����Ӧ�������ӷ���ʽΪCO32- + CO2 + H2O �� 2HCO3- ����3����A��B��C��Ϊ����ͬ�ֽ���Ԫ�صĻ����A��B��C�ֱ�Ϊ���Ρ�������������ƫ�����Σ�X��ǿ���Ӧ�������ӷ���ʽΪAl��OH��3 + OH- �� AlO2- + 2H2O����4����AΪ����Fe��XΪϡ���ᣬ��BΪ�����Σ�CΪ���Σ���Ӧ�������ӷ���ʽΪ3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O������B����Һ�м�������������Һ������Fe��OH��2�����ڿ���������������Ϊ�Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����Ӧ�Ļ�ѧ����ʽΪ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3 ����5����A��X��Ϊ���ʣ�BΪ��ʹƷ����Һ��ɫ�����壬B�Ƕ�������A����C������������Ӧ���Ļ�ѧ����ʽΪ
����2����A��B��CΪ��ɫ��Ӧ���ʻ�ɫ�Ļ����A��B��C�ֱ�ΪNa2O2 ��Na2O ��Na2CO3��NaHCO3��XΪ��ɫ��ζ���壬XΪCO2����Ӧ�������ӷ���ʽΪCO32- + CO2 + H2O �� 2HCO3- ����3����A��B��C��Ϊ����ͬ�ֽ���Ԫ�صĻ����A��B��C�ֱ�Ϊ���Ρ�������������ƫ�����Σ�X��ǿ���Ӧ�������ӷ���ʽΪAl��OH��3 + OH- �� AlO2- + 2H2O����4����AΪ����Fe��XΪϡ���ᣬ��BΪ�����Σ�CΪ���Σ���Ӧ�������ӷ���ʽΪ3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O������B����Һ�м�������������Һ������Fe��OH��2�����ڿ���������������Ϊ�Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����Ӧ�Ļ�ѧ����ʽΪ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3 ����5����A��X��Ϊ���ʣ�BΪ��ʹƷ����Һ��ɫ�����壬B�Ƕ�������A����C������������Ӧ���Ļ�ѧ����ʽΪ![]() ��
��

 ����Ӣ��ϵ�д�
����Ӣ��ϵ�д� ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д�