题目内容
根据表中信息,判断以下叙述正确的是:
A、氢化物的沸点为H2T<H2R B、单质与盐酸反应的速率为:L<Q
C、M与T形成的化合物具有两性 D、L2+与R2-的核外电子数相等
| 短周期元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.061 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
C、M与T形成的化合物具有两性 D、L2+与R2-的核外电子数相等
C
试题分析:根据原子半径和主要化合价可知L是Mg,M是Al,Q是Be,R是S,T是O,所以氢化物的沸点为H2O>H2S,单质与盐酸反应的速率为:Mg>Be,Al2O3具有两性,Mg2+与S2-的核外电子数不相等。答案选C。
点评:本题属于简单题,是学生需要熟练掌握的关于元素周期律的规律。要把这几种未知元素推出来就可以分析判断。

练习册系列答案
相关题目
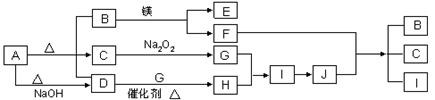

 反应中肯定不属于氧化还原反应的是 (填编号);
反应中肯定不属于氧化还原反应的是 (填编号);