题目内容
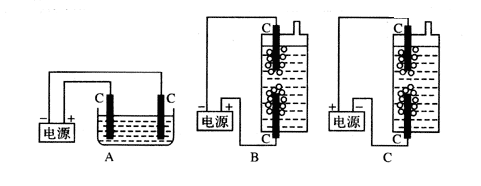
在密闭容器上,放入碳酸铵和氢氧化钠固体共A克,将容器加热至200℃,经充分反应后,排出其中的气体,冷却称得剩余固体的质量为B克。问容器内碳酸铵和氢氧化钠各多少克?
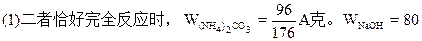
/176A克;
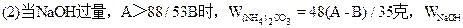
=(48B-13A)/35克;
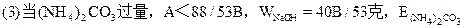
=A-40B/53克。
可能发生如下反应:
(NH4)2CO3+2NaOH 2NH3↑+Na2CO3 ①
2NH3↑+Na2CO3 ①
(NH4)2CO3 2NH3↑+CO2↑+H2O↑ ②
2NH3↑+CO2↑+H2O↑ ②
在加热过程中应首先发生反应①,只有当(NH4)2CO3过量时才能继续发生反应②。并由以上反应可看出,NaOH过量时减重少。下面分别讨论。
(1)当二者恰好反应时:
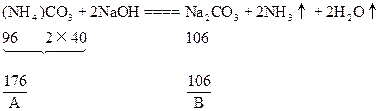
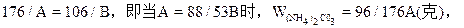
WNaOH=80/176A(克),(也可用B表示)。
(2)当NaOH过量,A>88/53B时,只发生反应①。先计算。(NH4)2CO3的量。
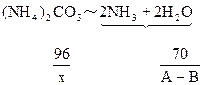
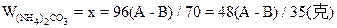
WNaOH=A-48(A-B)/53=(48B-13A)/35(克)
(3)当(NH4)2CO3过量,A<88/35B时,发生反应①、②。
但由②知(NH4)2CO3全分解无固体剩余,所以还由①式计算,先求NaOH的量。
2NaOH~Na2CO3
∴WNaOH=y=80B/106=40B/53(克),
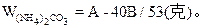
(NH4)2CO3+2NaOH
 2NH3↑+Na2CO3 ①
2NH3↑+Na2CO3 ①(NH4)2CO3
 2NH3↑+CO2↑+H2O↑ ②
2NH3↑+CO2↑+H2O↑ ②在加热过程中应首先发生反应①,只有当(NH4)2CO3过量时才能继续发生反应②。并由以上反应可看出,NaOH过量时减重少。下面分别讨论。
(1)当二者恰好反应时:
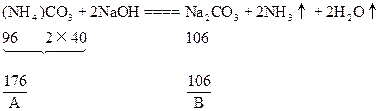
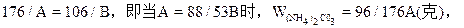
WNaOH=80/176A(克),(也可用B表示)。
(2)当NaOH过量,A>88/53B时,只发生反应①。先计算。(NH4)2CO3的量。
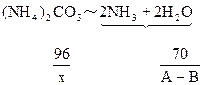
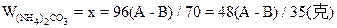
WNaOH=A-48(A-B)/53=(48B-13A)/35(克)
(3)当(NH4)2CO3过量,A<88/35B时,发生反应①、②。
但由②知(NH4)2CO3全分解无固体剩余,所以还由①式计算,先求NaOH的量。
2NaOH~Na2CO3
∴WNaOH=y=80B/106=40B/53(克),
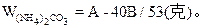

练习册系列答案
相关题目