题目内容
【题目】对已经达到平衡的反应 2X(g)+Y(g)![]() 2Z(g) ΔH<0 ,下列说法正确的是( )
2Z(g) ΔH<0 ,下列说法正确的是( )
A.缩小容器体积,正、逆反应速率都增大,平衡向逆反应方向移动
B.升高反应温度,该反应的平衡常数增大
C.改变条件使平衡正向移动,反应物的转化率一定都增大
D.加入催化剂,可以降低反应所需的活化能,但不改变反应的ΔH
【答案】D
【解析】
A.缩小容器体积,反应混合物的浓度增大,所以正、逆反应速率都增大,由于反应物的系数大于生成物的系数,所以正反应速率大于逆反应速率,所以化学平衡向正反应方向移动,A错误;
B.该反应的正反应是放热反应,升高反应温度,化学平衡向吸热的逆反应方向移动,所以该反应的平衡常数减小,B错误;
C.若是通过增大某种反应物的浓度使平衡正向移动,则其它反应物的转化率增大,而该反应物的转化率降低,C错误;
D.加入催化剂,可以改变反应途径,降低反应所需的活化能,但由于不能改变反应物、生成物的浓度,所以不改变反应的ΔH,D正确;
故合理选项是D。

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
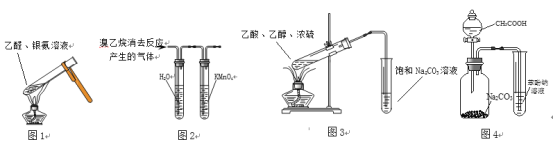
【题目】利用如图所示装置进行下列实验,不能达到相应实验目的的是( )
选项 | ① | ② | ③ | 实验目的 |
|
A | 稀硫酸 | Na2S | AgCl的浊液 | 验证Ag2S比AgCl难溶 | |
B | 浓硝酸 | Cu片 | NaOH溶液 | 探究浓硝酸具有氧化性 | |
C | 硫酸 | Na2SO3 | 酸性KMnO4溶液 | 探究SO2具有还原性 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 验证酸性:硝酸>碳酸>硅酸 |
A.AB.BC.CD.D