��Ŀ����
��1��������ͨ��ϡ��ˮ�У�NH3�����ϵ�һ��H��Clȡ�������Ȱ���Ȼ���������İ����Ȱ����ã��õ�������N2H4����д��������Ӧ�Ļ�ѧ����ʽ��_______________����2��������һ�ֿ�ȼ��Һ�壬���������ȼ�ϡ���֪32.0 gN2H4��H2O2��Ӧ���ɵ�����ˮ����̬�����ų�����642 kJ���÷�Ӧ���Ȼ�ѧ����ʽ�ǣ�_____________________________��
��3������������ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ������������ȼ�ϵ�طŵ�����N2��H2O����缫��Ӧʽ�ǣ�
������_____________________________________________________________��
������______________________________________________________________��
(1)NH3+Cl2====NH2Cl+HCl(��2NH3+Cl2====NH2Cl+NH4Cl),NH3+NH2Cl==== N2H4+HCl(��2NH3+NH2Cl====N2H4+NH4Cl)
(2)N2H4(l)+2H2O2(l)====N2(g)+4H2O(g);��H=-642 kJ/mol
(3)O2+2H2O+4e-====4OH- N2H4+4OH--4e-====4H2O+N2��
������������֪��Cl2+2NH3====NH2Cl+NH4Cl����NH2Cl+2NH3====N2H4+NH4Cl,NH4Cl����Ϊ���ɵ�HCl��NH3���ö����ɡ�N2H4��Һ�������ԣ�˵��N2H4�ܲ��ֵ������OH-����ӦΪN2H4+H2O![]()
![]() +OH-���Եڣ�3���ʣ�����������ȼ�ϵ�ص��ܷ�ӦΪN2H4+O2====N2+2H2O��O2�õ��ӣ�������������ӦʽΪO2+2H2O+4e-====4OH-��N2H4ʧ���ӱ��N2�������ĸ�����ӦΪ�����ܷ�Ӧ��ȥ������Ӧʽ��N2H4+4OH--4e-====N2��+4H2O��
+OH-���Եڣ�3���ʣ�����������ȼ�ϵ�ص��ܷ�ӦΪN2H4+O2====N2+2H2O��O2�õ��ӣ�������������ӦʽΪO2+2H2O+4e-====4OH-��N2H4ʧ���ӱ��N2�������ĸ�����ӦΪ�����ܷ�Ӧ��ȥ������Ӧʽ��N2H4+4OH--4e-====N2��+4H2O��

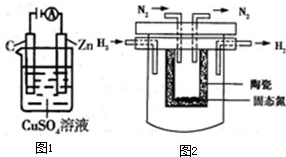

 ������N2H4����
������N2H4����