题目内容
【题目】合成导电高分子材料PPV的反应如下。下列说法正确的是( )
 +(2n-1)HI
+(2n-1)HI
A. 合成PPV的反应为加聚反应
B. 1molPPV最多能与4 molH2发生加成反应
C.  与溴水加成后的产物最多有14个原子共平面
与溴水加成后的产物最多有14个原子共平面
D.  和苯乙烯互为同系物
和苯乙烯互为同系物
【答案】C
【解析】
A、合成PPV通过缩聚反应生成,同时有小分子物质HI生成,不属于加聚反应,选项A错误;
B、1molPPV中含有2nmol碳碳双键,最多能与4n molH2发生加成反应,选项B错误;
C. 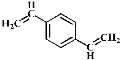 与溴水加成后的产物为
与溴水加成后的产物为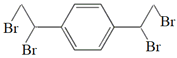 ,根据苯分子中12个原子共面、甲烷为正四面体结构可知,该分子中最多有14 个原子共平面,选项C正确;
,根据苯分子中12个原子共面、甲烷为正四面体结构可知,该分子中最多有14 个原子共平面,选项C正确;
D. 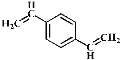 和苯乙烯相差C2H2,不是相差n个CH2,不互为同系物,选项D错误。
和苯乙烯相差C2H2,不是相差n个CH2,不互为同系物,选项D错误。
答案选C。

【题目】下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)写出下列元素的元素符号:①___,②___;
(2)在这些元素中,最活泼的金属元素是___,最不活泼的元素是___。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是___,碱性最强的是___,呈两性的氢氧化物是___。
(4)写出③和⑧的单质反应产物的电子式___。
(5)![]() C在周期表中的位置:第___周期___族,它与氧气完全燃烧的产物的电子式___。
C在周期表中的位置:第___周期___族,它与氧气完全燃烧的产物的电子式___。
(6)在③与④的单质中,化学性质较活泼的是___,判断的实验依据是___。
【题目】工业上常利用CO2为初始反应物,合成一系列重要的化工原料。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H1
NH2COONH4(s) △H1
反应Ⅱ:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H3=-86.98kJ/mol 请回答下列问题:
CO(NH2)2(s)+H2O(g) △H3=-86.98kJ/mol 请回答下列问题:
①根据8电子稳定构型,写出 CO(NH2)2的结构式_________________。
②反应Ⅰ的△H1=______________。
③在____(填“高温”或“低温”)情况下有利于反应Ⅱ的自发进行。
④一定温度下,在体积固定的密闭容器中按 n(NH3):n(CO2)=2:1 进行反应Ⅰ,下列能说明反应Ⅰ达到了平衡状态的是_______(填序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.NH3与CO2的转化率相等
D.容器内混合气体的密度不再变化
(2)将CO2和H2按质量比25:3充入一定体积的密闭容器中,在不同温度下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。
CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。

①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为K(Ⅰ)_____K(Ⅱ)(填“ >”“<”或“=”)。
②欲提高CH3OH的平衡产率,可采取的措施除改变温度外,还有__________________(任写两种)。
③一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物起始投入量 | 1molCO2、3molH2 | a molCO2、bmolH2、cmolCH3OH(g) |
c mol H2O(g) (a、b、c 均不为零) | ||
若甲容器平衡后气体的压强为开始的 5/6,则该温度下,反应的平衡常数为__________,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,乙容器中 c 的取值范围为_______。