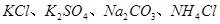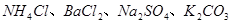题目内容
对某溶液进行下列操作,结论正确的是( )
| A、加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有CO32- | B、加入BaCl2溶液,生成白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有Ag+ | C、加入Ba(NO3)2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,则原溶液中一定有SO42- | D、加入NaOH溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝,则原溶液中一定有NH4+ |
分析:A.该气体为二氧化碳或者二氧化硫,原溶液中可能存在HSO3-、SO32-、HCO3-,不一定含有CO32-;
B.该白色沉淀可能为硫酸钡,原溶液中可能含有SO42-;
C.该白色沉淀可能为亚硫酸钡,原溶液中可能含有SO32-;
D.能使湿润的红色石蕊试纸变蓝的气体为氨气,则原溶液中一定含有铵根离子.
B.该白色沉淀可能为硫酸钡,原溶液中可能含有SO42-;
C.该白色沉淀可能为亚硫酸钡,原溶液中可能含有SO32-;
D.能使湿润的红色石蕊试纸变蓝的气体为氨气,则原溶液中一定含有铵根离子.
解答:解:A.加入盐酸,生成的气体能使澄清石灰水变浑浊,该气体可能为二氧化碳或二氧化硫,原溶液中可能存在HSO3-、SO32-、HCO3-,不一定有CO32-,故A错误;
B.加入BaCl2溶液,生成白色沉淀,再加稀盐酸,沉淀不消失,该白色沉淀可能为硫酸钡,原溶液中可能含有SO42-,不一定含有Ag+,故B错误;
C.加入Ba(NO3)2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,原白色沉淀可能为亚硫酸钡,加入稀硝酸后被氧化成硫酸钡,则原溶液中可能含有SO32-,不一定有SO42-,故C错误;
D.加入NaOH溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝,该气体一定为氨气,则原溶液中一定有NH4+,故D正确;
故选D.
B.加入BaCl2溶液,生成白色沉淀,再加稀盐酸,沉淀不消失,该白色沉淀可能为硫酸钡,原溶液中可能含有SO42-,不一定含有Ag+,故B错误;
C.加入Ba(NO3)2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,原白色沉淀可能为亚硫酸钡,加入稀硝酸后被氧化成硫酸钡,则原溶液中可能含有SO32-,不一定有SO42-,故C错误;
D.加入NaOH溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝,该气体一定为氨气,则原溶液中一定有NH4+,故D正确;
故选D.
点评:本题考查了常见离子的检验,题目难度中等,注意掌握常见离子的性质及正确的检验方法,明确检验离子的存在时,必须排除干扰离子,确保检验方案的严密性.

练习册系列答案
相关题目
(2011?咸阳模拟)某无色溶液中只可能含有Na+、Ba2+、Cl-、Br-、SO32-、SO42-,对该溶液进行下列实验,实验操作和现象如下表:
|
对某溶液进行下列操作,结论正确的是( )
| A、滴入酚酞,溶液变红,再做焰色反应火焰呈黄色,则原溶液中是氢氧化钠溶液 | B、逐滴加氢氧化钠溶液至过量,先生成沉淀后沉淀部分溶解,说明原溶液既有Mg2+又有Al3+ | C、加入Ba(NO3)2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,则原溶液中一定有SO42- | D、加入NaOH溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝,则原溶液中一定有NH4+ |
(16分)某化学兴趣小组在课外活动中,对某溶液进行了三次检验,每次检验结果如下表所示,请回答下列问题。
|
检验次数 |
溶液中检验出的物质 |
|
第一次 |
|
|
第二次 |
|
|
第三次 |
|
(1)三次检验结果中第 次检验结果不正确。
(2)检验时,为了证明溶液中存在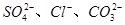 ,进行下列实验:(填写下列空白)
,进行下列实验:(填写下列空白)
|
步骤 |
实验操作 |
预期现象及结论 |
|
1 |
向溶液中滴加 (填化学式)溶液至过量 |
|
|
2 |
__________________________ __________________________ |
|
|
3 |
过滤,再向滤液中加入 ________(填化学式)溶液 |
|
(3)步骤1中溶液滴加过量的目的是__________________________________________
如何判断步骤2中的溶液已加过量_________________________________________