题目内容
【题目】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3,其流程如下:
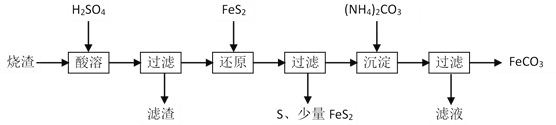
已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:FeS2 + 14Fe3+ + 8H2O =15Fe2+ + 2SO42— + 16H+
下列说法不正确的是
A. “还原”后可以用KSCN检验Fe3+是否反应完全
B. “还原”时反应Ⅱ的离子方程式为2Fe3+ + FeS2 = 2S↓+ 3Fe2+
C. “沉淀”时,可以先将溶液调节成强碱性,再加入(NH4)2CO3
D. 所得FeCO3需充分洗涤,可以用稀盐酸和BaCl2溶液检验FeCO3是否已洗涤干净
【答案】C
【解析】A. Fe3+可与KSCN 溶液反应生成血红色溶液,所以“还原”后可以用KSCN检验Fe3+是否反应完全,A正确;B.由题中信息可知,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ为FeS2 + 14Fe3+ + 8H2O =15Fe2+ + 2SO42— + 16H+,还原后过滤所得滤渣中含有S,所以 “还原”时反应Ⅱ的离子方程式为2Fe3+ + FeS2 = 2S↓+ 3Fe2+,B正确;C. “沉淀”时,若先将溶液调节成强碱性,则Fe2+转化为氢氧化亚铁,再加入(NH4)2CO3,得不到碳酸亚铁,C不正确;D. 所得FeCO3需充分洗涤,取最后一次洗涤液,用稀盐酸和BaCl2溶液检验洗涤液中是否含有SO42-,确定FeCO3是否已洗涤干净,D正确。本题选C。

练习册系列答案
相关题目