题目内容
硅酸酸性弱于碳酸。下列实验事实能证明此结论的是
| A.CO2溶于水形成碳酸,SiO2难溶于水 |
| B.CO2通入可溶性硅酸盐中析出硅酸沉淀 |
| C.高温下SiO2与碳酸盐反应生成CO2 |
| D.氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀 |
B
解析试题分析:依据较强的酸制取较弱的酸可知,B中CO2可以制取硅酸,这就说明硅酸的酸性弱于碳酸的酸性;A是溶解性和酸性强弱无关系;C中反应不是复分解反应,不能说明;D中只能说明硅酸和碳酸的酸性都弱于盐酸的,不正确,答案选B。
考点:考查酸性的强弱比较

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于SO2性质的分析,正确的是
| A.通入BaCl2溶液中,有白色沉淀生成 | B.通入FeCl3溶液中,有SO42-生成 |
| C.通入氯水中,有淡黄色沉淀生成 | D.通入KI溶液中,有I2生成 |
下列有关H2SO4的说法中正确的是
| A.将过量的Zn投入一定量的浓H2SO4中,最终生成的气体只有SO2 |
| B.向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 |
| C.运输保存浓硫酸的槽罐车一旦泄露后应立即用大量水冲洗 |
| D.向5 mL 18 mol·L-1的硫酸中加入足量铜片并加热使其充分反应,生成0.045 mol SO2 |
为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂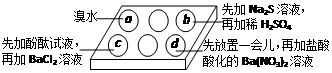
对实验现象的“解释或结论”错误的是
| 选项 | 实验现象 | 解释或结论 |
| A | a中溴水褪色 | 还原性:SO32—> Br— |
| B | b中加硫酸后产生淡黄色沉淀 | SO32—和S2—在酸性条件下发生反应 |
| C | c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪去 | SO32—+H2O HSO3—+OH—,所以滴入酚酞变红; HSO3—+OH—,所以滴入酚酞变红;Ba2++SO32—→BaSO3↓(白),使水解平衡左移,红色褪去 |
| D | d中产生白色沉淀 | Na2SO3溶液已被氧化变质 |
2013年3月,京沪高速公路一辆载有约35 t液氯的槽罐车与一辆货车相撞,导致槽罐车中液氯大面积泄漏,造成多人伤亡。下列处理方法和过程合理的是( )
| A.将人群转移到地势较低的地方,等待营救 |
| B.将槽罐车推入附近的水塘中,撒上石灰 |
| C.用高压水枪向空中喷洒大量酸性溶液 |
| D.被转移人群可戴上用NaOH处理过的口罩 |
有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列有关硅的说法中,不正确的是
| A.高纯度的硅广泛用于制作计算机芯片 |
| B.硅可由二氧化硅还原制得 |
| C.低温时,硅与水、空气和盐酸不反应,但能与氢氟酸反应 |
| D.自然界中硅的储量丰富,自然界中存在大量的单质硅 |
下列说法中正确的是
| A.向久置的氯水中滴入紫色石蕊试液,溶液先变红后褪色 |
| B.纯净的氢气在氯气中安静地燃烧,发出苍白色火焰 |
| C.漂白粉的有效成分是CaCl2和Ca(ClO)2,应密闭保存 |
| D.在氯气泄漏时,可以用浸有NaOH水溶液的毛巾捂住口鼻,并向下风方向跑 |
下列溶液通入过量CO2后,最终溶液中有沉淀析出的是
| A.Na2SO3 | B.BaCl2 | C.Ca(ClO)2 | D.NaAlO2 |
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
| A.再通入少量氯气,c(H+)/c(ClO-)减小 |
| B.通入少量SO2,溶液漂白性增强 |
| C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) |
| D.加入少量固体NaOH,溶液的pH会略微增大 |