题目内容
13.下列各组物质中分子数一定相同的是( )| A. | 标准状况下11.2L CO2和0.5 molCO2 | |
| B. | 18 mL H2O和2x10Pa,27C 16gO2 | |
| C. | 1 molCO和88gCO2 | |
| D. | 27℃,22.4 LCl2和含4mol氧原子的H2SO4 |
分析 A、标准状况下11.2L CO2物质的量为0.5mol,两的物质的量相等;
B、18 mL 的水质量为18g,物质的量为1mol,而16g的氧气的物质的量为$\frac{16g}{32g/mol}$=0.5mol;
C、88g的二氧化碳的物质的量为:$\frac{88g}{44g/mol}$=2mol;
D、不是标准无法由体积求物质的量.
解答 解:A、标准状况下11.2L CO2物质的量为0.5mol,两的物质的量相等,所以分子数相同,故A正确;
B、18 mL 的水质量为18g,物质的量为1mol,而16g的氧气的物质的量为$\frac{16g}{32g/mol}$=0.5mol,两者的物质的量不等,所以分子数不等,故B错误;
C、88g的二氧化碳的物质的量为:$\frac{88g}{44g/mol}$=2mol,两者的物质的量不等,所以分子数不等,故C错误;
D、不是标准无法由体积求物质的量,所以22.4 LCl2的物质的量不知,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.

练习册系列答案
相关题目
20.下列物质分离方法不正确的是( )
| A. | 用过滤的方法除去食盐水中的泥沙 | |
| B. | 用酒精萃取碘水中的碘 | |
| C. | 用分液的方法分离汽油和氯化钠溶液 | |
| D. | 用蒸馏的方法将自来水制成蒸馏水 |
4.下列有机化合物分子中,所有碳原子不可能处于同一平面的是( )
| A. |  | B. | CH3-C≡C-CH3 | C. | 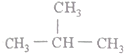 | D. | 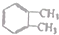 |
8.某化学小组通过査阅资料,设计了如图所示的方法以含镍催化剂为原料来制备NiSO4•7H20.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
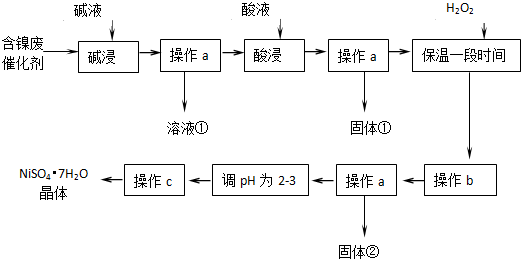
部分阳离子以氢氧化物形式沉淀时的pH如下:
(1)“碱浸”时反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2OH-═2AlO2-+H2O.
(2)“酸浸”时所加入的酸是H2SO4(填化学式).
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M═NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.

部分阳离子以氢氧化物形式沉淀时的pH如下:
| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
(2)“酸浸”时所加入的酸是H2SO4(填化学式).
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M═NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
18.下列各组物质中,互为同分异构体的是( )
| A. | 2-甲基丙烷 正丁烷 | B. | 氧气 臭氧 | ||
| C. | 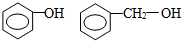 | D. | 金刚石 石墨 |
5.下列烷烃的命名错误的是( )
| A. | 3-甲基丁烷 | B. | 2-甲基-3-乙基戊烷 | ||
| C. | 2,2-二甲基丁烷 | D. | 2,3-二甲基丁烷 |
3.湿化学法(NPP-法)制备纳米级活性氧化锌,可以用氧化锌粗品(含有FeO、Fe2O3、CuO杂质)为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙烧获得活性氧化锌.其化学工艺流程如图:
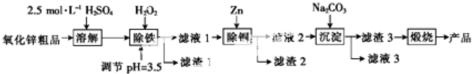
已知:溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表:
(1)实验室用98%浓H2SO4(ρ=1.84g/cm3)来配制100ml 2.5mol/L稀H2SO4所需的玻璃仪器有烧杯、胶头滴管、00mL容量瓶、量筒、玻璃棒.
(2)上述流程图中pH=12的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式,下同),滤渣2是Cu、Zn.加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.

已知:溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表:
| 离子 | 开始沉 淀的pH | 完全沉 淀的pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.7 | 3.2 |
| Cu2+ | 5.2 | 6.7 |
| Zn2+ | 6.8 | 9.0 |
(2)上述流程图中pH=12的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式,下同),滤渣2是Cu、Zn.加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.
 .
.