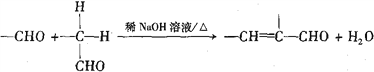
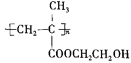
��Ŀ����
����Ŀ�������������ʹ�õĽ���֮һ�����������仯�����֪ʶ������������⣮
��1��������Ԫ�ؼ������������л�ԭ�Ե�������_______������ĸ�������
A��Fe B��FeCl3 C��FeSO4 D��Fe2O3
��2��ȡһ�����Ȼ��������壬���Ƴ�0.1 mol/L ����Һ���������������Ƿ������ķ�����______________________________________________��
������ҵ���ó�����Fe2O3��FeO��Ҳ����Al2O3��MnO2��CuO��SiO2�ȣ��Ʊ��̷�FeSO4��7H2O���������£�
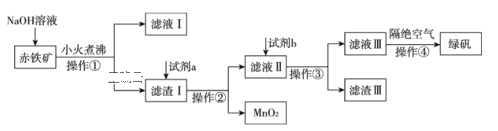
��1������������Һ����������з�����Ӧ�����ӷ���ʽΪ____________��_________________��
��2�����������м���������Լ�aΪ___________���������Լ�bͶ�뵽��Һ�����������з�Ӧ�����ӷ���ʽΪ______________��_________________��________________��
��3��ʵ�����в����٢ڢ۵�����Ϊ_________________________��
��4�������ܸ���������Ŀ����_______________________________________________��
��. ������أ�K2FeO4����һ�����͡���Ч�������ɫˮ����������Cl2��O2��ClO2��KMnO4�����Ը�ǿ��������Ⱦ����ҵ�������Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���KOH�����ͣ�ʹ�������������
��1���ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ��2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2�����÷�Ӧ��Na2O2 ��________��������������ԭ��������CO2��Ӧ�Ļ�ѧ��Ӧ����ʽ_________________________��
��2��ʪ���Ʊ�������صķ�Ӧ��ϵ������������Fe(OH)3��ClO����OH����FeO42-��Cl����H2O��
�ټ��������£��������ͻ�ԭ�������ʵ����ı�Ϊ3:2������Ӧ��д������ƽʪ���Ƹ�����ص����ӷ�Ӧ����ʽ��___________________________________________________________��
������Ӧ������ת����0.3mol���ӣ���ԭ��������ʵ���Ϊ____mol��
���𰸡�C ȡ������Һ���Թ��У����뼸��KSCN��Һ������Ѫ��ɫ������Fe3+���������ӱ����� Al2O3+2OH-=2AlO2��+H2O SiO2+2OH-=SiO32-+H2O ����(H2SO4) Fe��2Fe3+��3Fe2+ Fe��Cu2+��Cu��Fe2+ Fe��2H+��H2����Fe2+ ���� ��ֹ��Һ�е�Fe2+����������ΪFe3+ ����������ԭ�� 2Na2O2+2CO2 = 2Na2CO2+O2 2Fe��OH��3 + 3ClO- + 4OH- = 2FeO42- + 3Cl- + 5H2O 0.15
��������
I.��1��Ԫ�ػ��ϼ����ߣ�����ԭ�������л�ԭ�ԣ�Ԫ�ػ��ϼ۽��ͣ��������������������ԣ�
��2��ѡ��KSCN��Һ�ɼ���Fe3+�Ĵ��ڣ�
II. ������Fe2O3��FeO��Ҳ����Al2O3��MnO2��CuO��SiO2�ȣ������Ʊ����̿�֪����NaOH��Al2O3��SiO2��NaOH��Ӧ������ҺI�к�OH-��AlO2-��SiO32-������I�к�Fe2O3��FeO��MnO2��CuO�����Լ�aΪ���ᣬ�����٢ھ�Ϊ���ˣ���Һ���к����ᡢFe2��SO4��3��FeSO4��CuSO4���Լ�bΪFe��������Ϊ���ˣ�������ΪCu��Fe����Һ��FeSO4������Ũ������ȴ�ᾧ�õ��̷�FeSO4��7H2O���Դ������
��. ��1������������ԭ��Ӧ�л��ϼ����߱���������ԭ�������ϼ۽��ͱ���ԭ���������Ĺ��ɷ��������ֹ��������������̼����̼���ƺ�������
��2����ʪ���Ʊ�������أ�K2FeO4��ʱ��Fe(OH)3ʧ���ӱ���������K2FeO4����C1O-������������ԭ����C1-���������������ڼ��������´��ڣ����Ը÷�Ӧ���ڼ��������½��У��ٽ��ת�Ƶ����غ���ƽ����ʽ��
�ڸ��ݻ��ϼ۱仯�͵���ת�������������
I.��1��������Ԫ�ؼ������������л�ԭ�ԣ�Ӧ�ô����м��̬�����ϼۼȿ������ߣ��ֿ��Խ��ͣ�
A. Fe���ϼ���ͣ���������������A�������
B. FeCl3��Ԫ��Ϊ+3�ۣ�����ǿ�����ԣ�һ�������û�л�ԭ�ԣ���B�������
C. FeSO4����Ԫ��Ϊ+2�ۣ����������ֿɽ��ͣ���C��������⣻
D. Fe2O3��Ԫ��Ϊ+3�ۣ�����ǿ�����ԣ�һ�������û�л�ԭ�ԣ���D�����
��ѡC��
��2��Fe2+���ױ���������ΪFe3+��KSCN��Һ����Fe3+��Һ�Ժ�ɫ���ʼ������������Ƿ������ķ���Ϊ��ȡ������Һ���Թ��У����뼸��KSCN��Һ������Ѫ��ɫ������Fe3+��˵�����������ӱ�������
�ʴ�Ϊ��ȡ������Һ���Թ��У����뼸��KSCN��Һ������Ѫ��ɫ������Fe3+���������ӱ�������
II. ������Fe2O3��FeO��Ҳ����Al2O3��MnO2��CuO��SiO2�ȣ������Ʊ����̿�֪����NaOH��Al2O3��SiO2��NaOH��Ӧ������ҺI�к�OH-��AlO2-��SiO32-������I�к�Fe2O3��FeO��MnO2��CuO�������Լ�aΪ���ᣬ�����٢ھ�Ϊ���ˣ���Һ���к����ᡢFe2��SO4��3��FeSO4��CuSO4���Լ�bΪFe��������Ϊ���ˣ�������ΪCu��Fe����Һ��FeSO4������Ũ������ȴ�ᾧ�õ��̷�FeSO4��7H2O��
��1������������֪��Al2O3��SiO2����NaOH��Ӧ��������������Һ����������з�����Ӧ�����ӷ���ʽΪ��Al2O3+2OH-=2AlO2��+H2O��SiO2+2OH-=SiO32-+H2O��
�ʴ�Ϊ��Al2O3+2OH-=2AlO2��+H2O��SiO2+2OH-=SiO32-+H2O��
��2������ʵ��Ŀ�Ŀ�֪���Լ�aΪ���ᣬ��Fe2O3��FeO��CuO�������ϡ���ᷴӦ����Fe2+��Fe3+��Cu2+������Һ���к������������ᡢFe2(SO4)3��FeSO4��CuSO4��Ҫ��õ�FeSO4����ȥ������ϡ���ᡢFe2(SO4)3��CuSO4����Ҫ���뻹ԭ��Fe���ʹ������Լ�bͶ�뵽��Һ���������з�Ӧ�����ӷ���ʽΪ��Fe��2Fe3+��3Fe2+��Fe��Cu2+��Cu��Fe2+��Fe��2H+��H2����Fe2+��
�ʴ�Ϊ��Fe��2Fe3+��3Fe2+��Fe��Cu2+��Cu��Fe2+��Fe��2H+��H2����Fe2+��
��3
�ʴ�Ϊ�����ˣ�
��4���õ���FeSO4��Һ�ױ�����������Fe2(SO4)3��Ϊ��ֹFe2+����������ΪFe3+����Ҫ����������
�ʴ�Ϊ����ֹ��Һ�е�Fe2+����������ΪFe3+��
��. ��1����Ӧ��FeԪ�ػ��ϼ���+2������Ϊ+6�ۣ���������FeSO4Ϊ��ԭ��������������OԪ�صĻ��ϼ�һ����1�۽���Ϊ2�ۣ���һ����1������Ϊ0���������Ƽ���������Ҳ�ǻ�ԭ�������������������̼�ᷴӦ����̼�������������仯ѧ����ʽΪ��2Na2O2+2CO2 = 2Na2CO2+O2��
�ʴ�Ϊ������������ԭ����2Na2O2+2CO2 = 2Na2CO2+O2��
��2����ʪ���Ʊ����������K2FeO4��ʱ��Fe(OH)3ʧ���ӱ���������K2FeO4��Fe�Ļ��ϼ�������3����C1O������������ԭ����C1����Ԫ�صļ�̬����2�������ݵ����غ����õ���Ԫ������ǰ��ϵ����2��Cl��ǰ��ϵ����3���������������ڼ��������´��������Ը÷�Ӧ���ڼ��������½����������ӷ�ӦΪ2Fe(OH)3+3ClO+4OH�T2FeO42+3Cl+5H2O��
�ʴ�Ϊ��2Fe(OH)3+3ClO+4OH�T2FeO42+3Cl+5H2O��
�ڷ�Ӧ2Fe(OH)3+3ClO+4OH�T2FeO42+3Cl+5H2O��ת�Ƶ�����6 mol����ԭ����Ϊ�����ӡ����ݹ�ϵʽ6e-![]() 3 Cl��֪������Ӧ������ת����0.3 mol���ӣ���ԭ���������ӵ����ʵ���Ϊ0.15 mol���ʴ�Ϊ�� 0.15��
3 Cl��֪������Ӧ������ת����0.3 mol���ӣ���ԭ���������ӵ����ʵ���Ϊ0.15 mol���ʴ�Ϊ�� 0.15��