��Ŀ����
����Ŀ����������̼���º���{[Ni��CHZ��3]��ClO4��2 }��һ�����͵���ҩ��
��1��Ni2+��̬��������Ų�ʽΪ ��
��2��ClO4���Ŀռ乹��������ClO4����Ϊ�ȵ������һ�ַ���Ϊ���ѧʽ����
��3����ѧʽ��CHZΪ̼���£����ΪCO��N2H3��2 �� ̼������̼ԭ�ӵ��ӻ��������Ϊ��1molCO��N2H3��2�����к��ЦҼ���ĿΪ ��
��4����������̼���º�������NiO�������ἰ̼���»��϶��ɣ�NiO�ľ����ṹ��ͼ��ʾ�������к��е�Ni2+��ĿΪa��Ni2+����λ��Ϊb��NiO������ÿ�������Ӿ����������������ĿΪc����a��b��c= �� 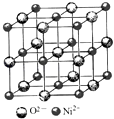
���𰸡�
��1��1s22s22p63s23p63d8
��2���������壻CCl4��
��3��sp2��11��6.02��1023
��4��2��3��6
���������⣺��1��NiԪ��ԭ�Ӻ�����28�����ӣ�ԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d84s2 �� Niʧȥ4s�ܼ�2�������γ�Ni2+ �� Ni2+���Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d8 �� ���Դ��ǣ�1s22s22p63s23p63d8����2��ClO4������ԭ�Ӽ۲���Ӷ���Ϊ4+ ![]() =4��û�йµ��Ӷԣ�����ռ乹���ǣ��������壻ԭ��������ͬ���۵���������ͬ������Ϊ�ȵ����壬��ClO4����Ϊ�ȵ������һ�ַ���ΪCCl4�ȣ����Դ��ǣ��������壻CCl4�ȣ���3��CO��N2H3��2��Cԭ����Oԭ��֮���γ�˫������Nԭ��֮���γ�C��N������û�й¶Ե��ӣ��ӻ������ĿΪ3��Cԭ�Ӳ�ȡsp2�ӻ�����N2H3�е�ԭ��֮���γ�N��N������Nԭ����Hԭ��֮���γ�N��H�����������к���11���Ҽ�����1molCO��N2H3��2�����к��ЦҼ���ĿΪ11��6.02��1023 �� ���Դ��ǣ�sp2��11��6.02��1023����4����Ni2+����λ�ھ������㼰���ģ�������Ni2+��Ŀx=8��
=4��û�йµ��Ӷԣ�����ռ乹���ǣ��������壻ԭ��������ͬ���۵���������ͬ������Ϊ�ȵ����壬��ClO4����Ϊ�ȵ������һ�ַ���ΪCCl4�ȣ����Դ��ǣ��������壻CCl4�ȣ���3��CO��N2H3��2��Cԭ����Oԭ��֮���γ�˫������Nԭ��֮���γ�C��N������û�й¶Ե��ӣ��ӻ������ĿΪ3��Cԭ�Ӳ�ȡsp2�ӻ�����N2H3�е�ԭ��֮���γ�N��N������Nԭ����Hԭ��֮���γ�N��H�����������к���11���Ҽ�����1molCO��N2H3��2�����к��ЦҼ���ĿΪ11��6.02��1023 �� ���Դ��ǣ�sp2��11��6.02��1023����4����Ni2+����λ�ھ������㼰���ģ�������Ni2+��Ŀx=8�� ![]() +6��
+6�� ![]() =4���Զ���Ni2+�����о�����֮�����O2������λ�����м��ҹ���Ni2+���ӶԳƣ���Ni2+����λ��y=6����֮�����Ni2+����λ�����ģ�ÿ������Ϊ12���湲�ã���֮�����������������Ŀz=12����x��y��z=4��6��12=2��3��6�����Դ��ǣ�2��3��6��
=4���Զ���Ni2+�����о�����֮�����O2������λ�����м��ҹ���Ni2+���ӶԳƣ���Ni2+����λ��y=6����֮�����Ni2+����λ�����ģ�ÿ������Ϊ12���湲�ã���֮�����������������Ŀz=12����x��y��z=4��6��12=2��3��6�����Դ��ǣ�2��3��6��






