题目内容
【题目】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。

请回答下列问题。
(1)B、C、D、E 4种物质的化学式为:
B____________、C____________、D____________、E____________。
(2)沉淀F与NaOH溶液反应的离子方程式为________________________________。
沉淀E与稀硫酸反应的离子方程为____________________________________。
溶液G与过量稀氨水反应的化学方程为________________________________。
【答案】 Al2O3 Fe2O3 NaAlO2 Al(OH)3 Al2O3+2OH-=2AlO2-+H2O Al(OH)3+3H+=Al3+ +3H2O Al2(SO4)3+6NH3·H2O=2Al(OH)3↓+3(NH4)2SO4
【解析】本题考查无机推断,Al2(SO4)3溶于水,Al2O3和Fe2O3是不溶于水的物质,因此A中加水,过滤,沉淀F为Al2O3和Fe2O3的混合物,溶液G为Al2(SO4)3,氧化铝属于两性氧化物,Fe2O3属于碱性氧化物,因此F中加入NaOH发生Al2O3+2NaOH=2NaAlO2+H2O,然后过滤,沉淀C为Fe2O3,溶液D为NaAlO2,溶液G中加入过量的稀氨水,发生Al3++3NH3·H2O=Al(OH)3↓+3NH4+,沉淀E为Al(OH)3,氢氧化铝不稳定受热分解为Al2O3,即B为Al2O3, (1)根据上述分析,B为Al2O3,C为Fe2O3,D为NaAlO2,E为Al(OH)3;(2)沉淀F为氧化铝和氧化铁的混合物,氧化铁属于碱性氧化物,不与NaOH反应,氧化铝属于两性氧化物,与NaOH反应:Al2O3+2OH-=2AlO2-+H2O;氢氧化铝为两性氢氧化物,与硫酸反应的离子反应方程式为:Al(OH)3+3H+=Al3++3H2O;硫酸铝与过量氨水的反应化学方程式为Al2(SO4)+6NH3·H2O=2Al(OH)3↓+3(NH4)2SO4。

 金牌教辅培优优选卷期末冲刺100分系列答案
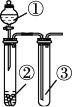
金牌教辅培优优选卷期末冲刺100分系列答案【题目】利用如图所示装置进行下列实验,能达到实验目的的是 ( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓硫酸 | 铜 | 溴水 | 验证浓硫酸具有强氧化性 | |
B | 浓盐酸 | 浓硫酸 | 空气 | 制取并收集HCl | |
C | 浓氨水 | 氧化钙 | 空气 | 制取并收集NH3 | |
D | 稀硫酸 | Na2CO3 | Na2SiO3 溶液 | 验证酸性:硫酸>碳酸>硅酸 |
A. A B. B C. C D. D