题目内容
12. 物质间的三角转化关系是化学中常见关系,如图所示,已知A、B、C都含有同一种元素X,且A、B、C之间可以相互转化.
物质间的三角转化关系是化学中常见关系,如图所示,已知A、B、C都含有同一种元素X,且A、B、C之间可以相互转化.(1)若A是常见金属的氢氧化物,且A+OH-→B,A+H+→C,写出:①B→C的离子方程式AlO2-+4H+=Al3++2H2O.
②由C制备A的离子方程式Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(2)若A是酸性氧化物,是正常雨水pH=5.6的原因,B、C的焰色反应为黄色,相同条件下B的溶解度小于C的溶解度.则A的电子式是
 ,B的俗名是小苏打.
,B的俗名是小苏打.写出:C在溶液中转化为B的化学方程式Na2CO3+CO2+H2O=2NaHCO3.
分析 (1)若A是常见金属的氢氧化物,且A+OH-→B,A+H+→C,可知A为两性氢氧化物,应为Al(OH)3,由转化关系可知B为AlO2-,C为Al3+;
(2)若A是酸性氧化物,是正常雨水pH=5.6的原因,应为CO2,B、C的焰色反应为黄色,说明含有钠元素,相同条件下B的溶解度小于C的溶解度,则B为NaHCO3,C为Na2CO3,以此解答该题.
解答 解:(1)若A是常见金属的氢氧化物,且A+OH-→B,A+H+→C,可知A为两性氢氧化物,应为Al(OH)3,由转化关系可知B为AlO2-,C为Al3+,
①B→C的离子方程式为AlO2-+4H+=Al3++2H2O,故答案为:AlO2-+4H+=Al3++2H2O;
②由C制备A,可有铝盐与氨水反应生成,反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(2)若A是酸性氧化物,是正常雨水pH=5.6的原因,应为CO2,电子式为 ,B、C的焰色反应为黄色,说明含有钠元素,相同条件下B的溶解度小于C的溶解度,则B为NaHCO3,俗称小苏打,C为Na2CO3,C在溶液中转化为B的化学方程式为Na2CO3+CO2+H2O=2NaHCO3,
,B、C的焰色反应为黄色,说明含有钠元素,相同条件下B的溶解度小于C的溶解度,则B为NaHCO3,俗称小苏打,C为Na2CO3,C在溶液中转化为B的化学方程式为Na2CO3+CO2+H2O=2NaHCO3,
故答案为: ;小苏打;Na2CO3+CO2+H2O=2NaHCO3.
;小苏打;Na2CO3+CO2+H2O=2NaHCO3.
点评 本题考查无机物的推断,为高考常见题型和高频考点,侧重于学生的分析能力的考查,题目难度不大,注意根据转化关系判断物质反应的类型,结合物质的特点进行解答,注意相关基础知识的积累.

练习册系列答案
相关题目
2.氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定,易分解;CuH在氯气中能燃烧;CuH跟盐酸反应能产生气体.以下有关推断中不正确的是( )
| A. | “另一种反应物”在反应中表现还原性 | |
| B. | CuH在化学反应中既可做氧化剂也可做还原剂 | |
| C. | CuH在氯气中燃烧的化学方程式为CuH+Cl2$\frac{\underline{\;点燃\;}}{\;}$CuCl+HCl | |
| D. | CuH与盐酸反应生成的气体是H2 |
3. 某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光.下列有关该电池的说法正确的是( )
某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光.下列有关该电池的说法正确的是( )
 某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光.下列有关该电池的说法正确的是( )
某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光.下列有关该电池的说法正确的是( )| A. | 铜片上的电极反应:Cu2++2e-=Cu | |
| B. | 外电路中电子由铜片经导线流向锌片 | |
| C. | 电池工作时电能直接转化为化学能 | |
| D. | 该电池工作时,若有13克锌被溶解,则铜片上产生标况下4.48 LH2 |
20.下列各组的三种元素,属于同一周期的是( )
| A. | C、H、O | B. | Li、Na、K | C. | F、Cl、Br | D. | Si、P、S |
7.二氟二氯甲烷(CF2Cl2)是甲烷的一种取代物,下列关于它的说法正确的是( )
| A. | 它有四种同分异构体 | B. | 它有两种同分异构体 | ||
| C. | 它只有一种结构 | D. | 它是平面分子 |
17.下列叙述正确的是( )
| A. | 分子中一定含有共价键 | B. | 共价化合物中可能含有离子键 | ||
| C. | 离子化合物中可能含有共价键 | D. | 离子化合物中只含有离子键 |
1.下列叙述正确的是( )
| A. | 硫酸钡难溶于水,故硫酸钡为弱电解质 | |
| B. | 石墨虽能导电,但不是电解质,而是非电解质 | |
| C. | 反应热只与反应体系的始态和终态有关,而与反应的途径无关 | |
| D. | 所有的放热反应都能在常温常压下自发进行 |
 (加聚反应)
(加聚反应) (取代反应)
(取代反应) (取代反应)
(取代反应) ;若
;若 若在上述类似条件下发生反应,请写出反应的方程式
若在上述类似条件下发生反应,请写出反应的方程式 .
.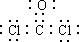 .为了防止发生事故,使用前要先检验氯仿是否变质,写出检验所用的试剂硝酸银溶液.
.为了防止发生事故,使用前要先检验氯仿是否变质,写出检验所用的试剂硝酸银溶液.