��Ŀ����
ʯ�ͻ����ǽ���ʡ��֧����ҵ֮һ��������ϩ���Ǻϳ�ά���ڵ���Ҫ���塣ij�������������з�Ӧԭ������������ϩ����2CH2=CH2+O2![]() 2CH3CHO ��
2CH3CHO ��
2CH3CHO+O2![]() 2CH3COOH ��
2CH3COOH ��
2CH2=CH2+2CH3COOH+O2![]() 2CH3COOCH=CH2+2H2O ��
2CH3COOCH=CH2+2H2O ��
���ڸ���Ӧ�ķ�������Ӧ������ϩ��������Ϊ75%����Ӧ������ȩ��������Ϊ80%����Ӧ�����������ϩ�������ʾ�Ϊ75%��
(1)Ϊʹ������ϩ���������������ϩ�Ⱥ����ε�Ͷ�ϱ�Ϊ���٣�
(2)��2.8��104 kg��ϩΪԭ�������Ƶô�����ϩ������ǧ�ˣ�
(3)�����������Ӧ�з�Ӧ�����ʵ���֮�Ⱦ�������Ӧ��ͬ������ϩ�Ϳ���Ϊԭ������������ϩ����ͨ��Ŀ���(O2���������Ϊ����1/5)����ϩ�����������Ϊ���٣�
(1)����ϩ����Ϊ1 mol���ڢٲ���Ӧ������ϩΪx mol
��ڢڲ�������CH3COOHΪx��75%��80%=0.6x
![]()
x=![]() ,1-x=
,1-x=![]() ��������Ͷ�ϱ�Ϊ5��3��
��������Ͷ�ϱ�Ϊ5��3��
![]()
m(CH3COOCHCH2)=1��106��![]() ��75%��86 g��mol-1=2.42��107 g=2.42��104 kg
��75%��86 g��mol-1=2.42��107 g=2.42��104 kg
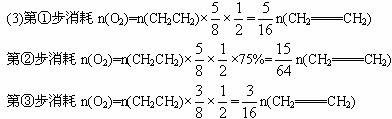
n(O2)��=![]() n(CH2=CH2)+
n(CH2=CH2)+ ![]() n(CH2=CH2)+
n(CH2=CH2)+ ![]() n(CH2=CH2)=
n(CH2=CH2)=![]() n(CH2=CH2)
n(CH2=CH2)
n(����)=![]() n(CH2=CH2)��
n(CH2=CH2)��![]() =
=![]() (CH2=CH2)
(CH2=CH2)
��:![]() =
=![]()

 ��100%)Ϊ98%����Ӧ��������ϩ���Ȼ���IJ��ʾ�Ϊ95%����2.8 t��ϩ���Ƶ�����ϩ__________t��ͬʱ�õ��������Ȼ���__________t��(����������1λС��)
��100%)Ϊ98%����Ӧ��������ϩ���Ȼ���IJ��ʾ�Ϊ95%����2.8 t��ϩ���Ƶ�����ϩ__________t��ͬʱ�õ��������Ȼ���__________t��(����������1λС��)