题目内容
【题目】“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用。它的有效成分是下列物质中的一种,这种物质是( )
A. NaOHB. NaClOC. KMnO4D. Na2O2
【答案】B
【解析】
“84”消毒液的主要成分是次氯酸钠,答案选B。

 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】在四个恒容密闭容器中按左下表相应量充入气体,发生2N2O(g) ![]() 2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如右下图所示,下列说法正确的是( )
2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如右下图所示,下列说法正确的是( )
容器 | 容积/L | 起始物质的量/L |
| ||
N2O | N2 | O2 | |||
I | V1 | 0.1 | 0 | 0 | |
II | 1.0 | 0.1 | 0 | 0 | |
III | V2 | 0.1 | 0 | 0 | |
IV | 1.0 | 0.06 | 0.06 | 0.04 | |
A. 该反应的正反应放热
B. 相同温度下反应时,平均反应速率:v(I)>v(Ⅲ)
C. 图中A、B、C三点处容器内总压强:V(III)<V(II)<V(I)
D. 容器IV在470℃进行反应时,起始速率:v(N2O)正<v(N2O)逆
【题目】某实验小组设计实验,利用酸性KMnO4溶液与H2C2O4溶液反应,测定溶液紫色消失所需时间的方法,研究浓度对反应速率的影响。供选择的实验药品有:0.01mol·L-1酸性KMnO4溶液、0.1mol·L-1酸性KMnO4溶液、0.1mol·L-1H2C2O4溶液、0.2mol·L-1H2C2O4溶液。
(1)H2C2O4溶液与酸性KMnO4溶液反应的化学方程式为____________________________。
(2)请完成以下实验设计表。
实验 | 酸性KMnO4溶液 | H2C2O4溶液 | 褪色 时间/s | ||
c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
甲 | 0.01 | 4 | 0.1 | 2 | t1 |
乙 | a | 4 | b | 2 | t2 |
①表中a=________、b=________;
②甲组实验KMnO4的平均反应速率是:____________(用含t1的式子表示)。
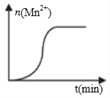
(3)测得某次实验(恒温)时,溶液中Mn2+物质的量与时间关系如图。请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因:______。