题目内容
【题目】某小组依据氧化还原反应:2Ag+(aq)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原电池如图所示,下列说法正确的是
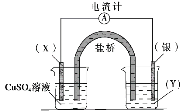
A.电极X可以是碳棒也可以是银棒
B.盐桥中的阳离子流向CuSO4溶液所在烧杯
C.银电极为电池的负极,发生的电极反应为Ag-e-=Ag+
D.外电路中电流的方向是从银电极流向X电极
【答案】D
【解析】
由方程式2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)可知,反应中Ag+被还原,为正极反应,则电解质溶液Y为硝酸银溶液,Cu被氧化,为原电池负极,则X为Cu,据此分析解答。
A.根据上述分析,电极X为铜,故A错误;
B.X为负极,银为正极,盐桥中的阳离子流向Y溶液所在烧杯,故B错误;
C.根据上述分析,银电极为电池的正极,发生的电极反应为Ag++e-=Ag,故C错误;
D.X为负极,银为正极,外电路中电流的方向是从银电极流向X电极,故D正确;
故选D。

练习册系列答案
相关题目