题目内容
Ⅰ.玻璃棒是中学化学实验室中常用的仪器.下列实验过程中,一般不需要用玻璃棒的是①用pH试纸测定Na2CO3溶液的pH
②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)28H20晶体和NH4Cl晶体反应过程中的能量变化
⑤用蒸馏法分离两种沸点差距较大的液体
⑥过滤分离互不相溶的固体和液体
⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程
⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案.
[方案一]准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量.
(1)此方案中,酸碱中和滴定时应选用
(2)写出此方案中涉及到的反应的离子方程式
[方案二]准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量.
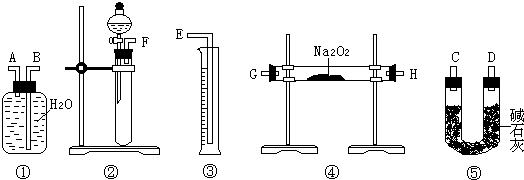
(3)该方案的实验过程中,如图,仪器的连接顺序是
(4)装置⑤的作用是
(5)你认为方案一、方案二中测定结果比较准确的是
分析:Ⅰ溶解固体时搅拌是加速溶解的,过滤时是引流作用,测溶液酸碱性或测PH值用玻璃棒蘸取待测液,蒸发时搅拌防止局部温度过高使液滴飞溅,配制一定体积的物质的量浓度的溶液用玻璃棒引流;
Ⅱ(1)根据用已知浓度的盐酸进行滴定;
(2)Na2O和Na2O2能与水反应生成氢氧化钠;
(3)测定某含有杂质Na2O的Na2O2样品的纯度,根据过氧化钠与水反应生成氧气,通过测定氧气的体积测量过氧化钠的质量,进而计算含量;
(4)根据碱石灰能吸收二氧化碳分析;
(5)方案二中,装置中的气体不一定全部赶出.
Ⅱ(1)根据用已知浓度的盐酸进行滴定;
(2)Na2O和Na2O2能与水反应生成氢氧化钠;
(3)测定某含有杂质Na2O的Na2O2样品的纯度,根据过氧化钠与水反应生成氧气,通过测定氧气的体积测量过氧化钠的质量,进而计算含量;
(4)根据碱石灰能吸收二氧化碳分析;
(5)方案二中,装置中的气体不一定全部赶出.
解答:解:Ⅰ)①用pH试纸测定Na2CO3溶液的pH,可应玻璃棒蘸取溶液,故需要;
②配制一定物质的量浓度的氯化钠溶液,可用玻璃棒搅拌、引流,故需要;
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体,不能用玻璃棒搅拌,防止胶体聚沉,故不需要;
④探究Ba(OH)2?8H2O晶体和NH4Cl晶体反应过程中的能量变化,可用玻璃棒搅拌,以使反应充分进行,故需要;
⑤用蒸馏法分离两种沸点差距较大的液体需要在蒸馏烧瓶中蒸馏分离,无需玻璃棒;
⑥过滤分离互不相溶的固体和液体,需用玻璃棒引流;
⑦用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验,此处无需用玻璃棒;
⑧稀释浓H2SO4的过程,为防止放出大量的热而使液体飞溅,用玻璃棒搅拌.
故答案为:③⑤⑦;
Ⅱ(1)用已知浓度的盐酸进行滴定,应用酸式滴定管,故答案为:酸式;
(2)Na2O和Na2O2能与水反应生成氢氧化钠,氢氧化钠能与盐酸反应:Na2O+H2O=2Na++2OH-;2Na2O2+2H2O=4Na++4OH-+O2↑;H++OH-=H2O,
故答案为:Na2O+H2O=2Na++2OH-;2Na2O2+2H2O=4Na++4OH-+O2↑;H++OH-=H2O;
(3)测定某含有杂质Na2O的Na2O2样品的纯度,方法是制备二氧化碳气体,与过氧化钠反应,生成的气体通过碱石灰的干燥管,用排水法测量氧气的体积,根据氧气的体积便可知样品中过氧化钠的质量,排水法测定氧气的体积时,导管应短进长出,故答案为:②④⑤①③;A;
(4)氧气中混有二氧化碳气体,为准确测量生成的氧气的体积,应用碱石灰吸收二氧化碳,故答案为:除去O2中混有的CO2等气体;
(5)方案二中,装置中的气体不一定全部赶出,误差较大,故答案为:方案一.
②配制一定物质的量浓度的氯化钠溶液,可用玻璃棒搅拌、引流,故需要;
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体,不能用玻璃棒搅拌,防止胶体聚沉,故不需要;
④探究Ba(OH)2?8H2O晶体和NH4Cl晶体反应过程中的能量变化,可用玻璃棒搅拌,以使反应充分进行,故需要;
⑤用蒸馏法分离两种沸点差距较大的液体需要在蒸馏烧瓶中蒸馏分离,无需玻璃棒;
⑥过滤分离互不相溶的固体和液体,需用玻璃棒引流;
⑦用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验,此处无需用玻璃棒;
⑧稀释浓H2SO4的过程,为防止放出大量的热而使液体飞溅,用玻璃棒搅拌.
故答案为:③⑤⑦;
Ⅱ(1)用已知浓度的盐酸进行滴定,应用酸式滴定管,故答案为:酸式;
(2)Na2O和Na2O2能与水反应生成氢氧化钠,氢氧化钠能与盐酸反应:Na2O+H2O=2Na++2OH-;2Na2O2+2H2O=4Na++4OH-+O2↑;H++OH-=H2O,
故答案为:Na2O+H2O=2Na++2OH-;2Na2O2+2H2O=4Na++4OH-+O2↑;H++OH-=H2O;
(3)测定某含有杂质Na2O的Na2O2样品的纯度,方法是制备二氧化碳气体,与过氧化钠反应,生成的气体通过碱石灰的干燥管,用排水法测量氧气的体积,根据氧气的体积便可知样品中过氧化钠的质量,排水法测定氧气的体积时,导管应短进长出,故答案为:②④⑤①③;A;
(4)氧气中混有二氧化碳气体,为准确测量生成的氧气的体积,应用碱石灰吸收二氧化碳,故答案为:除去O2中混有的CO2等气体;
(5)方案二中,装置中的气体不一定全部赶出,误差较大,故答案为:方案一.
点评:本题考查物质的组成和含量的测量,题目较为综合,难度较大,注意把握实验方案的设计原理.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目