题目内容
某一元弱酸(用HA表示)在水中的电离方程式是:HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向 (填“正”、“逆”)反应方向移动,理由是 。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向 (填“正”、“逆”、“不移动”)反应方向移动,溶液中c(A-)将 (填“增大”、“减小”或“不变”,下同),溶液中c(OH-)将 。
 H++A-,回答下列问题:
H++A-,回答下列问题:(1)向溶液中加入适量NaA固体,以上平衡将向 (填“正”、“逆”)反应方向移动,理由是 。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向 (填“正”、“逆”、“不移动”)反应方向移动,溶液中c(A-)将 (填“增大”、“减小”或“不变”,下同),溶液中c(OH-)将 。
(1)逆 c(A-)增大,平衡向减小c(A-)的方向即逆反应方向移动 (2)正 减小 增大
(1)向溶液中加入适量NaA固体后,c(A-)增大,平衡向逆反应方向移动。
(2)氯化钠不参与反应,但溶液体积增大,平衡向正反应方向移动。溶液中c(A-)和氢离子浓度将减小,所以溶液中c(OH-)将增大。
(2)氯化钠不参与反应,但溶液体积增大,平衡向正反应方向移动。溶液中c(A-)和氢离子浓度将减小,所以溶液中c(OH-)将增大。

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
 2NH3,下列说法能表明该反应达到平衡状态的是( )
2NH3,下列说法能表明该反应达到平衡状态的是( ) Y+Z,其化学反应速率随时间变化的图像如图所示,其中t1时刻达到平衡,t2时刻缩小容器体积,t3时刻重新达到平衡,下列有关说法不正确的是( )
Y+Z,其化学反应速率随时间变化的图像如图所示,其中t1时刻达到平衡,t2时刻缩小容器体积,t3时刻重新达到平衡,下列有关说法不正确的是( )
 3Z(g),若反应开始时充入2mol X和2mol Y,达平衡后Y的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后Y的体积分数>a%的是
3Z(g),若反应开始时充入2mol X和2mol Y,达平衡后Y的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后Y的体积分数>a%的是 N2O4在一定体积中达平衡的标志是( )
N2O4在一定体积中达平衡的标志是( ) CO2(aq),CO2(aq)+H2O
CO2(aq),CO2(aq)+H2O 3C(气),不能标志反应达到平衡的是
3C(气),不能标志反应达到平衡的是 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表: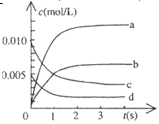
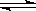 Ur﹣(尿酸根离子)+H3O+ Ur﹣(溶液)+Na+(溶液)
Ur﹣(尿酸根离子)+H3O+ Ur﹣(溶液)+Na+(溶液)