题目内容
下表中各组物质之间不能通过一步反应实现右图转化的是
| | 甲 | 乙 | 丙 |
| A | CH2=CH2 | CH3CH2Cl | CH3CH2OH |
| B | SiO2 | H2SiO3 | Na2SiO3 |
| C | Cl2 | HCl | CuCl2 |
| D | AlCl3 | Al(OH)3 | Al2O3 |

B
解析试题分析:A、甲与氯化氢加成得乙,乙分别发生消去反应、水解反应得甲、丙,丙发生消去反应得甲,正确;B、二氧化硅不能一步生成硅酸,错误;C、氯气与氢气反应生成氯化氢,浓盐酸与二氧化锰反应制得氯气,氯化氢溶液与氧化铜反应得氯化铜,电解氯化铜溶液得氯气,正确;D、氯化铝与氨水反应得氢氧化铝,氢氧化铝分解得氧化铝,氢氧化铝与盐酸反应得氯化铝,氧化铝与盐酸反应得氯化铝,正确,答案选B。
考点:考查物质之间的相互转化

练习册系列答案
相关题目
微粒甲与离子乙在溶液中的转化关系如下图所示:微粒甲是( )
| A.Si | B.Na+ | C.Al | D.SO2 |
将一定量的氯气通入30mL浓度为10.00 mol·L-1的NaOH浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是
| A.与NaOH反应的氯气一定为0.3mol |
| B.n(Na+):n(Cl-)可能为7:3 |
| C.若反应中转移的电子为n mol ,则0.15<n<0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
向x mL 2.0 mol·L-1的盐酸中投入a g镁铝合金,金属完全溶解,再加入y mL 1.0 mol·L-1的NaOH溶液沉淀达到最大值,且质量为(a+1.7) g,则下列说法不正确的是
| A.x=2y |
| B.镁铝合金与盐酸反应时转移电子的数目为0.1NA |
| C.镁铝合金与盐酸反应产生H2的体积在常温常压下大于1.12 L |
| D.a的取值范围为0.9 g<a<1.2 g |
下列物质的转化在给定条件下能实现的是
①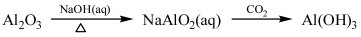
②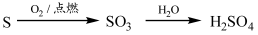
③
④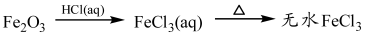
⑤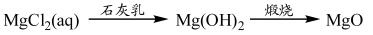
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
下列说法正确的是
| A.铝热反应是炼铁最常用的方法 |
| B.高纯度的硅单质用于制作光导纤维 |
| C.二氧化氯具有强化性,可用于自来水的杀菌消毒 |
| D.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
工业上用铝土矿(主要成分为Al2O3,含SiO2、Fe2O3等杂质)为原料冶炼铝的工艺流程如下,对下述流程中的判断正确的是: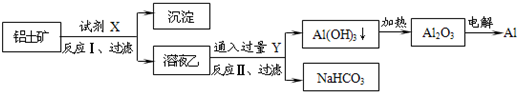
| A.试剂X为稀硫酸,沉淀中含有硅的化合物 |
| B.反应II中生成Al(OH)3的反应为:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
| C.结合质子(H+)的能力由弱到强的顺序是OH->CO32->AlO2- |
| D.Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al |
下列关于钠及其化合物的叙述正确的是 ( )。
| A.将足量的Na2O2和Na2O分别加入酚酞试液中,最终溶液均为红色 |
| B.用钠与空气反应制纯净的Na2O2,空气必须经过碱石灰处理后,才能与钠反应 |
| C.钠与钠离子都具有强还原性 |
| D.在Na2O2与CO2的反应中,氧化剂是Na2O2,还原剂是CO2 |