题目内容
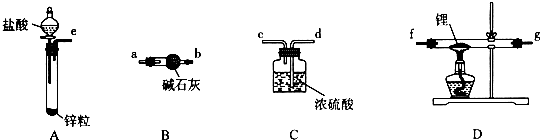
1. 莫尔盐[(NH4)2SO4•FeSO4•6H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用如图所示的实验装置来制取莫尔盐,实验步骤如下:
莫尔盐[(NH4)2SO4•FeSO4•6H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用如图所示的实验装置来制取莫尔盐,实验步骤如下:①用30%的NaOH溶液和废铁屑混合、煮沸、冷却、分离,将分离出的NaOH溶液装入F中;
②在E中用①处理过的铁屑和稀H2SO4反应制取FeSO4;
③将②制得的FeSO4溶液与(NH4)2SO4溶液混合,结晶得到莫尔盐.
试回答下列问题:
(1)利用铁屑和稀硫酸反应产生的氢气赶走装置中的氧气及硫酸铵溶液中溶解的氧,其目的是防止亚铁盐被氧化;
铁屑和稀硫酸反应产生的氢气的另外一个作用是将FeSO4溶液压至(NH4)2SO4溶液中.
(2)设计一个简单的实验证明产品中有Fe2+将少许所得晶体放入KSCN溶液不变色,再向溶液中加入氯水后变成血红色..
(3)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定.若取产品24.50g配成100mL溶液,取出10mL用0.10mol•L-1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL.
①试配平反应的离子方程式:
1MnO${\;}_{4}^{-}$+5Fe2++8H+=5Fe3++1Mn2++4H2O
②试求产品中莫尔盐的质量分数80.00% (NH4)2SO4•FeSO4•6H2O的相对分子质量为392).
分析 (1)由装置图可知,容器E的长导管插入液面以下,氢气只能从容器E的短导管出来,经过容器F加向容器D中.通入氢气排尽装置内空气,防止Fe2+氧化;当关闭BC,打开A时,E中气压增大,液体被压入D中,即将FeSO4溶液压至(NH4)2SO4溶液中;
(2)根据遇KSCN溶液呈血红色是Fe3+的特征反应,所以先加KSCN溶液,确定是否含有Fe3+;如果没有Fe3+,根据氯水的性质,再向溶液中加入氯水,观察溶液的颜色是否变化,从而确定是否含有Fe2+;
(3)①依据氧化还原反应电子守恒、电荷收、原子守恒配平写出离子方程式;
②根据关系式5Fe2+~MnO4-计算24.50g产品中Fe2+的物质的量,由(NH4)2SO4•FeSO4•6H2O可知Fe2+的物质的量等于莫尔盐的物质的量,再根据m=nM计算莫尔盐的质量,利用质量分数定义计算.
解答 解:(1)由装置图可知,向容器F中通入氢气,应关闭活塞A,打开活塞B、C.硫酸铵溶液中的溶解O2,容器D液面上部有O2,Fe2+易被氧化为Fe3+,通入氢气赶走硫酸铵溶液中的溶解O2和容器D液面上部的O2,防止Fe2+被氧化为Fe3+;F中的NaOH溶液的主要作用是除去混在氢气中的酸性气体;当关闭活塞B、C,打开A时,E中随着氢气的量的增大,气压增大,E中的液体被压入D中,即将FeSO4溶液压至(NH4)2SO4溶液中,
故答案为:防止亚铁盐被氧化;将FeSO4溶液压至(NH4)2SO4溶液中;
(2)将少许所得晶体放入KSCN溶液不变色,说明没有Fe3+,再向溶液中加入氯水后变成血红色,则含有Fe2+,
故答案为:将少许所得晶体放入KSCN溶液不变色,再向溶液中加入氯水后变成血红色;
(3)①高锰酸钾与Fe2+的反应是MnO4-~Mn2+~5e-;Fe2+~Fe3+~e-;依据电子守恒,铁离子和亚铁离子前乘5,依据原子守恒和电荷守恒得到反应的离子方程式为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
故答案为:1、5、8、1、5、4;
②假设24.50g产品中Fe2+的物质的量为xmol,则:
5Fe2+~~~~~~MnO4-,
5 1
xmol 0.01L×0.1000mol/L×10
所以x=$\frac{0.01L×0.1000mol/L×10×5}{1}$=0.05mol.
所以24.50g产品中(NH4)2SO4•FeSO4•6H2O的为0.05mol,
所以24.50g产品中(NH4)2SO4•FeSO4•6H2O的质量为0.05mol×392g/mol=19.6g.
所以24.50g产品中(NH4)2SO4•FeSO4•6H2O的质量分数为$\frac{19.6g}{24.50g}$×100%=80%.
故答案为:80%.
点评 本题以莫尔盐的制备为载体,考查实验原理与装置的理解分析与评价、氧化还原反应滴定应用以计算,题目难度中等.需学生具有扎实的基础知识与灵活运用知识解决问题的能力.注意(3)中计算,容易忽略所取溶液体积,为易错点.

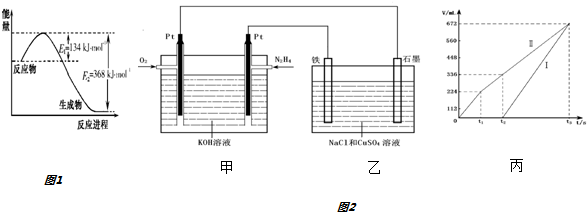
(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图.则反应过程中放出的总热量应为234kJ.
(2)在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的 关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②试判断K1>K2(填写“>”“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)=3v(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)化合物N2 H4 做火箭发动机的燃料时,与氧化剂N2O4反应生成N2和水蒸气.
某同学设计了一个N2H4--空气碱性燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图2所示.
①该燃料电池的负极反应式为N2H4+4OH--4e-=N2↑+4H2O;
②理论上乙中两极所得气体的体积随时间变化的关系如丙图中曲线 I、II所示(气体体积已换算成标准状况下的体积),写出在t1-t2时间段铁电极上的电极反应式Cu2++2e-=Cu;原混合溶液中NaCl的物质的量浓度为0.1mol/L
③在t2时所得溶液的pH为1.(假设溶液体积不变)
| A. | 物质发生化学变化都伴随着能量变化 | |
| B. | 任何反应中的能量变化都表现为热量变化 | |
| C. | 伴有能量变化的物质变化都是化学变化 | |
| D. | 在一个确定的化学反应体系中,反应物的总能量总是高于生成物的总能量 |
| A. | 12C和14C | B. | H2O和D2O | C. | O2和O3 | D. | 淀粉和纤维素 |
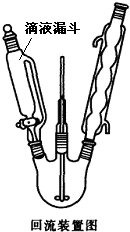 间硝基苯胺(Mr=128)是一种重要的染料中间体.它是一种黄色针状结晶,微溶于水,随温度升高溶解度增大,溶于乙醇、乙醚、甲醇.间硝基苯胺可选用间二硝基苯与碱金属多硫化物进行选择性还原,其反应式如下:
间硝基苯胺(Mr=128)是一种重要的染料中间体.它是一种黄色针状结晶,微溶于水,随温度升高溶解度增大,溶于乙醇、乙醚、甲醇.间硝基苯胺可选用间二硝基苯与碱金属多硫化物进行选择性还原,其反应式如下: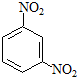 +Na2S2+H2O→
+Na2S2+H2O→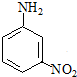 +Na2S2O3
+Na2S2O3