题目内容
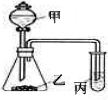
某化学学习小组利用右图所示装置来探究相应物质的化学性质的顺序.选择适当试剂完成实验A、B、C,并得出相应的
实验结论.实验A、B、C所用试剂或所得结论列于下表中.
(1)乙装置的名称
(2)请填写①~⑤的试剂名称或实验结论:
①
(3)小明利用该装置自行设计了一个实验--证明NO2具有氧化性(注:丙中已事先添加Na2S溶液).据此回答下列问题:
①如何检验该装置的气密性:
②打开甲装置的活塞后,装置乙中发生反应的化学方程式为:
③某同学对小明的实验设计提出了质疑,认为丙中溶液变浑浊不足以证明NO2具有氧化性,你认为他的理由是:
④NO2气体有毒,应用NaOH溶液吸收,请写出此反应的离子方程式:

实验结论.实验A、B、C所用试剂或所得结论列于下表中.
| 序 号 |
实验药品 | 实验结论 | ||
| 甲 | 乙 | 丙 | ||
| A | ① | 二氧化锰 | ② | 氧化性:O2>S |
| B | 醋酸溶液 | 碳酸钠溶液 | 硅酸钠溶液 | ③ |
| C | ④ | ⑤ | 氯化铝溶液 | 碱性:NaOH>NH3.H2O>Al(OH)3 |
锥形瓶
锥形瓶
. (2)请填写①~⑤的试剂名称或实验结论:
①
双氧水(过氧化氢溶液)
双氧水(过氧化氢溶液)
②氢硫酸溶液
氢硫酸溶液
③酸性:醋酸>碳酸>硅酸
酸性:醋酸>碳酸>硅酸
④浓氢氧化钠溶液(或饱和氢氧化钠溶液)
浓氢氧化钠溶液(或饱和氢氧化钠溶液)
⑤氯化铵固体(晶体)
氯化铵固体(晶体)
(3)小明利用该装置自行设计了一个实验--证明NO2具有氧化性(注:丙中已事先添加Na2S溶液).据此回答下列问题:
①如何检验该装置的气密性:
关闭分液漏斗的活塞,在丙中注一定量的水,将导管插入水中,微热锥形瓶,一段时间后在导管口看到有气泡产生,撤去酒精灯,在导管中产生一段水柱,说明装置的气密性良好
关闭分液漏斗的活塞,在丙中注一定量的水,将导管插入水中,微热锥形瓶,一段时间后在导管口看到有气泡产生,撤去酒精灯,在导管中产生一段水柱,说明装置的气密性良好
;②打开甲装置的活塞后,装置乙中发生反应的化学方程式为:
Cu+4HNO3=Cu(NO3)2+2NO2?+2H2O
Cu+4HNO3=Cu(NO3)2+2NO2?+2H2O
;③某同学对小明的实验设计提出了质疑,认为丙中溶液变浑浊不足以证明NO2具有氧化性,你认为他的理由是:
3NO2+H2O=2HNO3+NO,NO2和水反应生成的HNO3是一种强氧化性的酸,也可将Na2S氧化,也可使溶液变浑浊
3NO2+H2O=2HNO3+NO,NO2和水反应生成的HNO3是一种强氧化性的酸,也可将Na2S氧化,也可使溶液变浑浊
;(用化学反应方程式和简要文字回答)④NO2气体有毒,应用NaOH溶液吸收,请写出此反应的离子方程式:
2NO2+2OH-=NO3-+NO2-+H2O
2NO2+2OH-=NO3-+NO2-+H2O
.分析:(1)根据常用的仪器及图中所指来回答仪器的名称;
(2)根据结论和药品相结合,利用氧化剂的氧化性大于氧化产物的氧化性、强酸制取弱酸、强碱制取弱碱来分析;
(3)①该装置中有分液漏斗,应先关闭活塞,再利用微热法来检验装置的气密性;
②利用反应物与生成物及质量守恒定律来书写化学反应方程式;
③利用NO2和水反应的生成物来分析;
④利用NO2气体应用NaOH溶液吸收及氮元素的自身氧化还原反应来书写化学反应方程式.
(2)根据结论和药品相结合,利用氧化剂的氧化性大于氧化产物的氧化性、强酸制取弱酸、强碱制取弱碱来分析;
(3)①该装置中有分液漏斗,应先关闭活塞,再利用微热法来检验装置的气密性;
②利用反应物与生成物及质量守恒定律来书写化学反应方程式;
③利用NO2和水反应的生成物来分析;
④利用NO2气体应用NaOH溶液吸收及氮元素的自身氧化还原反应来书写化学反应方程式.
解答:解:(1)由图可知,乙为锥形瓶,故答案为:锥形瓶;
(2)A组中氧化性:O2>S,则乙中发生制取氧气的反应,丙中发生氧气与硫化物的反应,则①为双氧水(过氧化氢溶液),②为氢硫酸溶液;
B中乙和丙中都发生强酸制取弱酸的反应,则③为酸性:醋酸>碳酸>硅酸;
C中由碱性:NaOH>NH3.H2O>Al(OH)3,则乙、发生强碱与铵盐制取氨气的反应,则④为浓氢氧化钠溶液(或饱和氢氧化钠溶液),⑤为氯化铵固体(晶体),
故答案为:双氧水(过氧化氢溶液);氢硫酸溶液;酸性:醋酸>碳酸>硅酸;浓氢氧化钠溶液(或饱和氢氧化钠溶液);氯化铵固体(晶体);
(3)①由图可知,检验气密性应先关闭分液漏斗的活塞,在丙中注一定量的水,将导管插入水中,微热锥形瓶,一段时间后在导管口看到有气泡产生,撤去酒精灯,在导管中产生一段水柱,说明装置的气密性良好,
故答案为:关闭分液漏斗的活塞,在丙中注一定量的水,将导管插入水中,微热锥形瓶,一段时间后在导管口看到有气泡产生,撤去酒精灯,在导管中产生一段水柱,说明装置的气密性良好;
②该实验证明NO2具有氧化性,则乙中为制取二氧化氮的反应,则利用反应Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O来制取,故答案为:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;
③因二氧化氮与水反应生成的硝酸也具有氧化性,则在溶液中利用NO2来将Na2S氧化不严密,
故答案为:3NO2+H2O=2HNO3+NO,NO2和水反应生成的HNO3是一种强氧化性的酸,也可将Na2S氧化,也可使溶液变浑浊;
④NO2气体应用NaOH溶液吸收,氮元素发生自身氧化还原反应,生成硝酸钠和亚硝酸钠,则离子反应为2NO2+2OH-=NO3-+NO2-+H2O,故答案为:2NO2+2OH-=NO3-+NO2-+H2O.
(2)A组中氧化性:O2>S,则乙中发生制取氧气的反应,丙中发生氧气与硫化物的反应,则①为双氧水(过氧化氢溶液),②为氢硫酸溶液;
B中乙和丙中都发生强酸制取弱酸的反应,则③为酸性:醋酸>碳酸>硅酸;
C中由碱性:NaOH>NH3.H2O>Al(OH)3,则乙、发生强碱与铵盐制取氨气的反应,则④为浓氢氧化钠溶液(或饱和氢氧化钠溶液),⑤为氯化铵固体(晶体),
故答案为:双氧水(过氧化氢溶液);氢硫酸溶液;酸性:醋酸>碳酸>硅酸;浓氢氧化钠溶液(或饱和氢氧化钠溶液);氯化铵固体(晶体);
(3)①由图可知,检验气密性应先关闭分液漏斗的活塞,在丙中注一定量的水,将导管插入水中,微热锥形瓶,一段时间后在导管口看到有气泡产生,撤去酒精灯,在导管中产生一段水柱,说明装置的气密性良好,
故答案为:关闭分液漏斗的活塞,在丙中注一定量的水,将导管插入水中,微热锥形瓶,一段时间后在导管口看到有气泡产生,撤去酒精灯,在导管中产生一段水柱,说明装置的气密性良好;
②该实验证明NO2具有氧化性,则乙中为制取二氧化氮的反应,则利用反应Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O来制取,故答案为:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;
③因二氧化氮与水反应生成的硝酸也具有氧化性,则在溶液中利用NO2来将Na2S氧化不严密,
故答案为:3NO2+H2O=2HNO3+NO,NO2和水反应生成的HNO3是一种强氧化性的酸,也可将Na2S氧化,也可使溶液变浑浊;
④NO2气体应用NaOH溶液吸收,氮元素发生自身氧化还原反应,生成硝酸钠和亚硝酸钠,则离子反应为2NO2+2OH-=NO3-+NO2-+H2O,故答案为:2NO2+2OH-=NO3-+NO2-+H2O.
点评:本题为实验题,考查学生对氧化还原反应及强酸制取弱酸等实验的设计,本题的难度是实验设计证明NO2具有氧化性.

练习册系列答案
相关题目
某化学学习小组利用右图所示装置来探究相应物质的化学性质的顺序.选择适当试剂完成实验A、B、C,并得出相应的
实验结论.实验A、B、C所用试剂或所得结论列于下表中.
| 序 号 | 实验药品 | 实验结论 | ||
| 甲 | 乙 | 丙 | ||
| A | ① | 二氧化锰 | ② | 氧化性:O2>S |
| B | 醋酸溶液 | 碳酸钠溶液 | 硅酸钠溶液 | ③ |
| C | ④ | ⑤ | 氯化铝溶液 | 碱性:NaOH>NH3.H2O>Al(OH)3 |
(2)请填写①~⑤的试剂名称或实验结论:
①______ ②______③______④______ ⑤______
(3)小明利用该装置自行设计了一个实验--证明NO2具有氧化性(注:丙中已事先添加Na2S溶液).据此回答下列问题:
①如何检验该装置的气密性:______;
②打开甲装置的活塞后,装置乙中发生反应的化学方程式为:______;
③某同学对小明的实验设计提出了质疑,认为丙中溶液变浑浊不足以证明NO2具有氧化性,你认为他的理由是:______;(用化学反应方程式和简要文字回答)
④NO2气体有毒,应用NaOH溶液吸收,请写出此反应的离子方程式:______.
某化学学习小组利用右图所示装置来探究相应物质的化学性质的顺序.选择适当试剂完成实验A、B、C,并得出相应的
实验结论.实验A、B、C所用试剂或所得结论列于下表中.
(1)乙装置的名称______.
(2)请填写①~⑤的试剂名称或实验结论:
①______ ②______③______④______ ⑤______
(3)小明利用该装置自行设计了一个实验--证明NO2具有氧化性(注:丙中已事先添加Na2S溶液).据此回答下列问题:
①如何检验该装置的气密性:______;
②打开甲装置的活塞后,装置乙中发生反应的化学方程式为:______;
③某同学对小明的实验设计提出了质疑,认为丙中溶液变浑浊不足以证明NO2具有氧化性,你认为他的理由是:______;(用化学反应方程式和简要文字回答)
④NO2气体有毒,应用NaOH溶液吸收,请写出此反应的离子方程式:______.

实验结论.实验A、B、C所用试剂或所得结论列于下表中.
| 序 号 | 实验药品 | 实验结论 | ||
| 甲 | 乙 | 丙 | ||
| A | ① | 二氧化锰 | ② | 氧化性:O2>S |
| B | 醋酸溶液 | 碳酸钠溶液 | 硅酸钠溶液 | ③ |
| C | ④ | ⑤ | 氯化铝溶液 | 碱性:NaOH>NH3.H2O>Al(OH)3 |
(2)请填写①~⑤的试剂名称或实验结论:
①______ ②______③______④______ ⑤______
(3)小明利用该装置自行设计了一个实验--证明NO2具有氧化性(注:丙中已事先添加Na2S溶液).据此回答下列问题:
①如何检验该装置的气密性:______;
②打开甲装置的活塞后,装置乙中发生反应的化学方程式为:______;
③某同学对小明的实验设计提出了质疑,认为丙中溶液变浑浊不足以证明NO2具有氧化性,你认为他的理由是:______;(用化学反应方程式和简要文字回答)
④NO2气体有毒,应用NaOH溶液吸收,请写出此反应的离子方程式:______.
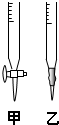 某化学学习小组的同学欲探究测定草酸晶体(H2C2O4?xH2O)中x的值.通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.该组同学利用该反应原理设计了滴定的方法测定x值.
某化学学习小组的同学欲探究测定草酸晶体(H2C2O4?xH2O)中x的值.通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.该组同学利用该反应原理设计了滴定的方法测定x值.