题目内容
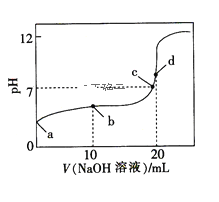
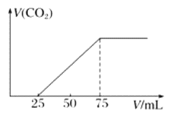
【题目】标准状况下,某气态烃A的密度是1.25g·L-1,取x L的A在足量的氧气中充分燃烧,生成的混合气体通入到50mLNaOH溶液,随后取此溶液25mL将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L-1的HCl溶液,产生的CO2气体体积与所加入的盐酸的体积之间的关系如图所示:
(1)A的摩尔质量为________________。
(2)请计算x的值(写出具体计算过程)。________________
【答案】28g·mol-1 该气态烃的摩尔质量为28g/mol,则该烃为乙烯C2H4,由图可知,当生成CO2气体时,发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,n(NaHCO3)=n(HCl)=0.05L×0.1mol·L-1=0.005mol,根据C元素守恒知,乙烯燃烧生成0.01mol CO2,则n(C2H4)=![]() n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。
n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。
【解析】
(1)根据公式![]() 进行计算;
进行计算;
(2)先确定该气态烃的分子式,再根据所发生的反应,结合图像,利用元素守恒进行计算。
(1)标准状况下,某气态烃A的密度是1.25g·L-1,则A的摩尔质量为![]() ;
;
(2)该气态烃的摩尔质量为28g/mol,则该烃为乙烯C2H4;取x L乙烯在足量的氧气中充分燃烧,生成二氧化碳和水蒸气,将该混合气体通入到50mLNaOH溶液中,CO2与NaOH溶液反应;随后取此溶液25mL将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L-1的HCl溶液,生成CO2气体,当生成CO2气体时,应发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,由图可知,生成CO2气体至体积最大,消耗HCl为50mL,则n(NaHCO3)=n(HCl)=0.05L×0.1mol·L-1=0.005mol,根据C元素守恒知,乙烯燃烧生成0.01mol CO2,则n(C2H4)=![]() n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。
n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。

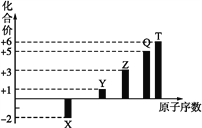
【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性.![]() 称为拟卤素,性质与卤素相似.下列说法不正确的是( )
称为拟卤素,性质与卤素相似.下列说法不正确的是( )
M | N | ||
X | Y |
A.X位于三周期IIA,其单质可采用电解熔融![]() 制备
制备
B.元素最高价氧化物的水化物中,酸性最强的是![]()
C.气体分子![]() 的电子式为
的电子式为![]()
D.![]() 其与氢氧化钠溶液反应的化学方程式为
其与氢氧化钠溶液反应的化学方程式为![]()