题目内容
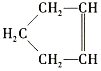
【题目】苯乙烯是一种重要的有机化工原料,其结构简式为![]() ,它一般不可能具有的性质是( )
,它一般不可能具有的性质是( )
A.难溶于水,易溶于有机溶剂,在空气中燃烧产生黑烟
B.分子中的所有原子一定在同一平面内
C.它能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D.能发生加成反应,在一定条件下最多可与四倍物质的量的氢气加成
【答案】B
【解析】
A. 苯乙烯属于烃类,难溶于水,易溶于有机溶剂,其分子式为C8H8,碳的含量较高,在空气中燃烧产生黑烟,A不符合题意;
B. 苯乙烯是一个苯基取代乙烯的一个氢,或一个乙烯基取代苯的一个氢形成的,乙烯所有原子共平面,苯的所有原子共平面,但由于乙烯和苯环相连接的是单键,它是可以任意旋转的,所以苯乙烯中所以原子可能在同一平面内,也可能不在同一平面内,B符合题意;
C. 含有碳碳双键,可与溴的四氯化碳溶液发生加成反应使之褪色,可被酸性高锰酸钾氧化使酸性高锰酸钾溶液褪色,C不符合题意;
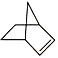
D. 1mol 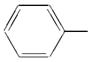 能与3mol H2发生加成反应,1mol
能与3mol H2发生加成反应,1mol  能与1mol H2发生加成反应,故与四倍物质的量的氢气发生加成反应,D不符合题意;
能与1mol H2发生加成反应,故与四倍物质的量的氢气发生加成反应,D不符合题意;
故答案为:B。

 名校课堂系列答案
名校课堂系列答案【题目】富马酸亚铁,是一种治疗缺铁性贫血的安全有效的铁制剂。富马酸在适当的pH条件下与FeSO4反应得富马酸亚铁。
已知:
物质名称 | 化学式 | 相对分子质量 | 电离常数(25℃) |
富马酸 | C4H4O4 | 116 | K1=9.5×10-4,K2=4.2×10-5 |
碳酸 | H2CO3 | K1=4.4×10-7,K2=4.7×10-11 | |
富马酸亚铁 | FeC4H2O4 | 170 |
i.制备富马酸亚铁:
①将富马酸置于100 mL烧杯A中,加热水搅拌
②加入Na2CO3溶液10 mL使溶液pH为6.5~6.7。并将上述溶液移至100 mL容器B中
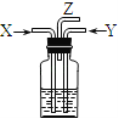
③安装好回流装置C,加热至沸。然后通过恒压滴液漏斗D缓慢加入FeSO4溶液30 mL
④维持反应温度100℃,充分搅拌1.5小时。冷却,减压过滤,用水洗涤沉淀
⑤最后水浴干燥,得棕红(或棕)色粉末,记录产量。
请回答以下问题:
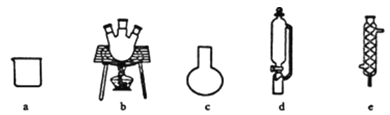
(1)该实验涉及到的主要仪器需从以下各项选择,则B为_________(填字母),C为___________(填名称);
(2)己知反应容器中反应物FeSO4和富马酸按恰好完全反应的比例进行起始投料,写出步骤②中加入Na2CO3溶液调节pH的目的是_____________,若加入Na2CO3溶液过量,对实验的影响是_____________;
(3)所需FeSO4溶液应现用现配,用FeSO4·7H2O固体配置FeSO4溶液的方法为:__________;
(4)写出容器B中制备富马酸亚铁的化学方程式:___________;
(5)步骤④检验沉淀是否洗净的方法是:________________;
ii. 计算产品的产率:
(6)经测定,产品中富马酸亚铁的纯度为76.5%、以5.80 g富马酸为原料反应制得产品8.50 g,则富马酸亚铁的产率为______________%(保留小数点后一位)。