题目内容
(2008?镇江二模)世界环保组织2006年度报告指出,人类已成功地使大气中氟氯烃减少,但C、N、S氧化物的排放有增无减,水资源的紧缺和污染加剧.
(1)大气中氟氯烃的减少带来的积极效应是
(2)酸雨的特征是pH<5.6,空气中硫氧化物和氮氧化物是形成酸雨的主要物质.
①若用NOX表示氮氧化物,请配平氮氧化物形成酸雨的化学方程式:
②酸雨落至地面后pH在一定时间内变小然后稳定于某一数值,原因是H2SO3受空气影响造成的,其化学方程式为:
(3)回收利用SO2既能减少大气污染,又能充分利用资源.已知:用Fe2+、Fe3+离子作催化剂,标况下在转化器中SO2可被O2氧化成SO42-,实现SO2 的回收利用.某同学设计测定转化器的脱硫效率方案如下:
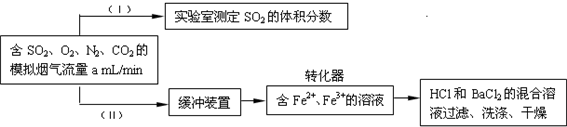
①在实验①(Ⅰ)中,为了确定SO2 的体积分数,可将模拟烟气缓慢通过已知体积和浓度的
②在标准状况下用实验(Ⅱ)测定转化器中的脱硫效率,若已知气流流速,还需测定的数据是
(1)大气中氟氯烃的减少带来的积极效应是
减缓臭氧层空洞的增大
减缓臭氧层空洞的增大
.(2)酸雨的特征是pH<5.6,空气中硫氧化物和氮氧化物是形成酸雨的主要物质.
①若用NOX表示氮氧化物,请配平氮氧化物形成酸雨的化学方程式:

②酸雨落至地面后pH在一定时间内变小然后稳定于某一数值,原因是H2SO3受空气影响造成的,其化学方程式为:
2H2SO3+O2=2H2SO4
2H2SO3+O2=2H2SO4
.(3)回收利用SO2既能减少大气污染,又能充分利用资源.已知:用Fe2+、Fe3+离子作催化剂,标况下在转化器中SO2可被O2氧化成SO42-,实现SO2 的回收利用.某同学设计测定转化器的脱硫效率方案如下:

①在实验①(Ⅰ)中,为了确定SO2 的体积分数,可将模拟烟气缓慢通过已知体积和浓度的
高锰酸钾溶液(或碘水和淀粉的混合液)
高锰酸钾溶液(或碘水和淀粉的混合液)
溶液,并用溶液的颜色刚好褪去时所消耗的模拟烟气的体积(标况下)来计算SO2 的体积分数.②在标准状况下用实验(Ⅱ)测定转化器中的脱硫效率,若已知气流流速,还需测定的数据是
实验时间
实验时间
和BaSO4的质量
BaSO4的质量
.分析:(1)从氟氯烃引起臭氧空洞的角度分析;
(2)关键在于分析出N元素化合价的变化值为(5-2x),O2中O元素化合价的变化值共为4,这样两者的最小公倍数为4(5-2x),很容易配平;
(3)①,只能利用SO2的还原性进行氧化还原滴定实验,如选择酸性高锰酸钾溶液或碘水和淀粉的混合溶液吸收SO2,这样,烟气中的O2、N2或CO2才没有干扰;
②要得到烟气的相关数据,必须借助气流流速和时间.
(2)关键在于分析出N元素化合价的变化值为(5-2x),O2中O元素化合价的变化值共为4,这样两者的最小公倍数为4(5-2x),很容易配平;
(3)①,只能利用SO2的还原性进行氧化还原滴定实验,如选择酸性高锰酸钾溶液或碘水和淀粉的混合溶液吸收SO2,这样,烟气中的O2、N2或CO2才没有干扰;
②要得到烟气的相关数据,必须借助气流流速和时间.
解答:解:(1)氟氯烃引起臭氧空洞,大气中氟氯烃的减少带来的积极效应应是减缓臭氧层空洞的增大,
故答案为:减缓臭氧层空洞的增大(或其它合理答案);
(2)①氧化还原反应中氧化剂和还原剂得失电子数目相等,在反应中,NOxN元素化合价的变化值为(5-2x),O2中O元素化合价的变化值共为4,
这样两者的最小公倍数为4(5-2x),则配平后的方程式为4NOx+(5-2x)O2+2H2O=4HNO3,
故答案为:4NOx+(5-2x)O2+2H2O=4HNO3;
②H2SO3具有氧化性,易被空气中氧气氧化为H2SO4,反应的方程式为2H2SO3+O2=2H2SO4,
故答案为:2H2SO3+O2=2H2SO4;
(3)①只能利用SO2的还原性进行氧化还原滴定实验,如选择酸性高锰酸钾溶液或碘水和淀粉的混合溶液吸收SO2,这样,烟气中的O2、N2或CO2才没有干扰,
故答案为:高锰酸钾溶液(或碘水和淀粉的混合液);
②要得到烟气的相关数据,必须借助气流流速和时间,需要根据BaSO4的质量测定二氧化硫的量,
故答案为:实验时间和BaSO4的质量.
故答案为:减缓臭氧层空洞的增大(或其它合理答案);
(2)①氧化还原反应中氧化剂和还原剂得失电子数目相等,在反应中,NOxN元素化合价的变化值为(5-2x),O2中O元素化合价的变化值共为4,
这样两者的最小公倍数为4(5-2x),则配平后的方程式为4NOx+(5-2x)O2+2H2O=4HNO3,
故答案为:4NOx+(5-2x)O2+2H2O=4HNO3;
②H2SO3具有氧化性,易被空气中氧气氧化为H2SO4,反应的方程式为2H2SO3+O2=2H2SO4,
故答案为:2H2SO3+O2=2H2SO4;
(3)①只能利用SO2的还原性进行氧化还原滴定实验,如选择酸性高锰酸钾溶液或碘水和淀粉的混合溶液吸收SO2,这样,烟气中的O2、N2或CO2才没有干扰,
故答案为:高锰酸钾溶液(或碘水和淀粉的混合液);
②要得到烟气的相关数据,必须借助气流流速和时间,需要根据BaSO4的质量测定二氧化硫的量,
故答案为:实验时间和BaSO4的质量.
点评:本题考查氧化还原反应的基本概念及其在生产、生活中的简单应用,难度中等,注意二氧化硫气体的性质以及氧化还原反应的有关知识.

练习册系列答案
相关题目



 F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) Fe(OH)3+3H+
Fe(OH)3+3H+